
【题目】有机化合物![]() 题目中所有物质中均无支链
题目中所有物质中均无支链![]() 在一定条件下具有如下所示的转化关系。
在一定条件下具有如下所示的转化关系。

回答:
(1)![]() 的结构简式为______,C和D的相互关系为______。
的结构简式为______,C和D的相互关系为______。
(2)指出下列转化的有机反应类型:![]() 属______类型;
属______类型;![]() 属______类型。
属______类型。
(3)生成B的反应方程式为:______。
(4)生成C的反应方程式为:______。
【答案】![]() 同分异构体 取代反应 消去反应 CH2OH(CH2)2COOH+CH3COOH
同分异构体 取代反应 消去反应 CH2OH(CH2)2COOH+CH3COOH ![]() CH3COOCH2CH2COOH+H2O CH2OH(CH2)2COOH
CH3COOCH2CH2COOH+H2O CH2OH(CH2)2COOH ![]() CH2=CHCH2COOH+H2O
CH2=CHCH2COOH+H2O
【解析】
由转化关系可知X含有羟基、羧基,且可形成五元环状化合物,结合B的分子式可知X应含有4个C原子,则X应为![]() ,由转化关系可知A为
,由转化关系可知A为![]() ,B为
,B为![]() ,C为
,C为![]() ,D为
,D为![]() ,以此解答该题。
,以此解答该题。
![]() 由以上分析可知X为
由以上分析可知X为![]() ,C为
,C为![]() ,D为
,D为![]() ,二者分子式相同,结构不同,互为同分异构体,
,二者分子式相同,结构不同,互为同分异构体,
故答案为:![]() ; 同分异构体;
; 同分异构体;
![]() 发生取代反应生成A,发生消去反应生成C,故答案为:取代反应;消去反应;
发生取代反应生成A,发生消去反应生成C,故答案为:取代反应;消去反应;
![]() 生成B的反应方程式为
生成B的反应方程式为![]() ,
,
故答案为:![]() ;
;
![]() 生成C的反应方程式为
生成C的反应方程式为![]() ,
,
故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列选项正确的是( )
A.25℃时,AgBr在0.0lmol/L的MgBr2溶液和NaBr溶液中的溶解度相同
B.53℃时,将0.01mol/L的醋酸溶液加水不断稀释,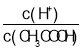 减小
减小
C.Na2CO3、NaHCO3溶液等浓度等体积混合后:3c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)]
D.NaCN溶液和盐酸混合呈中性的溶液中:c(Na+)>c(Cl-)=c(HCN)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
aA(g) |
| bB(g) |
| 2C(g) | |
起始物质的量浓度/(mol·L-1): | 1.5 | 1 | 0 | ||
2s末物质的量浓度/(mol·L-1): | 0.9 | 0.8 | 0.4 |
请回答下列问题。
①该可逆反应的化学方程式可表示为__。
②用物质B来表示0~2s的平均反应速率为__。
③从反应开始到2s末,A的转化率为__。
④下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是__(填序号)
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.vA:vB:vC=3:1:2
E.容器内气体C的物质的量分数保持不变
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn+O2=2ZnO。则该电池的负极材料是__。
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的示意图如图,该燃料电池工作时,电池的总反应方程式为__;负极的电极反应式为__。
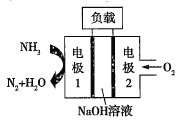
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容器中,能表示反应X(g)+2Y(g) ![]() 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比是1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
A. ①②B. ①④C. ②③D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7),工艺流程及相关物质溶解度曲线如图:
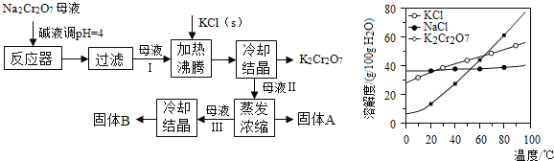
(1)由Na2Cr2O7生产K2Cr2O7的化学方程式为___________,通过冷却结晶析出大量K2Cr2O7的原因是___________.
(2)向Na2Cr2O7母液中加碱液调pH的目的是___________.
(3)固体A主要为___________(填化学式),固体B主要为___________(填化学式).
(4)用热水洗涤固体A,回收的洗涤液转移到母液___________(填“Ⅰ”“Ⅱ”或“Ⅲ”)中,既能提高产率又可使能耗最低。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应![]() 在5L的密闭容器中进行,0~30s内,C的物质的量增加了0.30mol。下列叙述正确的是( )
在5L的密闭容器中进行,0~30s内,C的物质的量增加了0.30mol。下列叙述正确的是( )
A.容器中D的物质的量至少为0.45mol
B.0~30s内,A的平均反应速率是0.010 mol·L-1·s-1
C.容器中A、B、C、D的物质的量之比一定是4:5:4:6
D.容器中A的物质的量一定增加了0.30mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种直接铁燃料电池(电池反应为:3Fe + 2O2=Fe3O4)的装置如图所示,下列说法正确的是

A. Fe极为电池正极
B. KOH溶液为电池的电解质溶液
C. 电子由多孔碳极沿导线流向Fe极
D. 每5.6gFe参与反应,导线中流过1.204×1023个e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A.甲烷燃烧热为890.3 kJmol-1,热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=+890.3 kJmolˉ1
B.稀盐酸和稀氢氧化钠溶液混合,其热化学方程式为:H++OH-=H2O △H=-57.3 kJmolˉ1
C.H2燃烧热为285.8kJmolˉ1,燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(1) △H=-571.6 kJmolˉ1
D.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6 kJ·mol-1
2NH3(g) △H=-38.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知A、B、C、D、E、F、G都是周期表中前四周期的元素,他们的原子序数依次增大。其中A原子的L层有2个未成对电子。D是电负性最大的元素,E与F同主族,E的二价阳离子与C的阴离子具有相同的电子层结构。G3+离子3d轨道电子为半满状态。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的順序为______________________。D的核外有______________种运动状态不同的电子。
(2)A的最简单氢化物属于___________(填“极性分子”和“非极性分子”)。![]() 离子空间构型是__________,其中心原子采取__________________杂化。
离子空间构型是__________,其中心原子采取__________________杂化。
(3)晶体熔点:EC_________FC(填“>”、“<”或“=”)
(4)G和M(质子数为25)两元素的部分电离能数据列于表:
元素 | M | G | |
电离能(kJmol-1) | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态M2+再失去一个电子比气态G2+再失去一个电子难。其原因是_________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com