
| Cu��Ag |
| �� |
| ˮԡ |
| ˮԡ |
| ���� |
| �� |
| ���� |
| �� |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
239 91 |
| A��330 | B��91 |
| C��239 | D��148 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
+ 4 |
2- 4 |
2- 3 |
| ʵ����� | ʵ������ | ʵ���� |
| a | ��AgNO3��Һ | �а�ɫ�������� |
| b | ������NaOH��Һ������ | �ռ�������1.12 L��������ɱ�״���µ������ |
| c | ������BaCl2��Һʱ�������ó�������ϴ�ӡ������������������м�����ϡ���ᣬȻ�������� | ��һ�γ�������Ϊ6.27 g���ڶ��γ�������Ϊ2.33 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� |
| �ŵ� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����Ϊ2L���ܱ������У�����lmol CO2��2.6mol H2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ?mol-1
�����Ϊ2L���ܱ������У�����lmol CO2��2.6mol H2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ?mol-1| n(CH3OH) |
| n(CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �û���Ӧ������ͼ��ʾ���ش��������⣺
�û���Ӧ������ͼ��ʾ���ش��������⣺
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
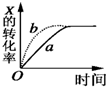 ��һ���¶��£���Ӧ��A��s��+3B��g����xC��g��+2D��g����һ��ѹ�����н��У�����˵������ȷ���ǣ�������
��һ���¶��£���Ӧ��A��s��+3B��g����xC��g��+2D��g����һ��ѹ�����н��У�����˵������ȷ���ǣ�������| A����λʱ��������n mol B��ͬʱ����n mol D����Ӧ������� |
| B���������������ʱ��˵����Ӧ�Ѵﵽƽ�� |
| C������Ӧʱ����������ӣ���x�ش���1�ҷ�Ӧһ��������� |
| D����x����1�����۷�Ӧ�Ƿ�ƽ�⣬����������������������ı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1mol?L-1 |
| B��0.25mol?L-1 |
| C��0.2mol?L-1 |
| D��0.5mol?L-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com