
(1)在标准状况下,200mL某气体的质量为1.142g,该气体的摩尔质量为
(2)已知某种混盐中含Na+、Mg2+、K+和Cl﹣离子物质的量分别为0.80mol、0.05mol、0.20mol和0.90mol.测知该混盐中还有SO42﹣,则SO42﹣物质的量为
(3)实验分析得知,200mL某硫酸铝溶液中含Al3+0.54g,求该溶液中硫酸根的物质的量浓度.
考点: 物质的量的相关计算.
专题: 计算题.
分析: (1)根据n=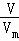 计算气体的物质的量,再根据M=
计算气体的物质的量,再根据M=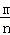 计算其摩尔质量;
计算其摩尔质量;
(2)溶液呈电中性,根据电荷守恒有:n(Na+)+2n(Mg2+)+n(K+)+n(Cl﹣)+2n(SO42﹣),据此解答;
(3)根据n=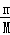 计算Al3+的物质的量,溶液中2n(SO42﹣)=3n(Al3+),再根据c=
计算Al3+的物质的量,溶液中2n(SO42﹣)=3n(Al3+),再根据c=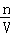 计算SO42﹣的物质的量浓度.
计算SO42﹣的物质的量浓度.
解答: 解:(1)200mL气体的物质的量为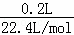 =
=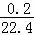 mol,其摩尔质量为
mol,其摩尔质量为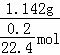 =128g/mol,故答案为:128g/mol;
=128g/mol,故答案为:128g/mol;
(2)溶液呈电中性,根据电荷守恒有:n(Na+)+2n(Mg2+)+n(K+)+n(Cl﹣)+2n(SO42﹣),即:0.8mol+0.05mol×2+0.20mol=0.90mol+2n(SO42﹣),解得n(SO42﹣)=0.1mol,故答案为:0.1mol;
(3)Al3+的物质的量为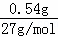 =0.02mol,溶液中2n(SO42﹣)=3n(Al3+),则SO42﹣的物质的量为0.02mol×
=0.02mol,溶液中2n(SO42﹣)=3n(Al3+),则SO42﹣的物质的量为0.02mol×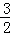 =0.03mol,SO42﹣的物质的量浓度为
=0.03mol,SO42﹣的物质的量浓度为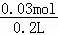 =0.15mol/L,
=0.15mol/L,
答:SO42﹣的物质的量浓度为0.15mol/L.
点评: 本题考查物质的量有关计算,难度不大,注意(2)中电解质混合溶液中离子物质的量计算经常利用电荷守恒计算.


科目:高中化学 来源: 题型:
小红在帮实验员整理化学试剂时,发现一瓶标签破损的无色溶液,标签严重破损,只能隐约看到一部分(如图).下列说法不正确的是( )

|
| A. | 该有机物肯定是甲酸乙酯,能发生银镜反应 |
|
| B. | 该有机物的分子式为C3H6O2 |
|
| C. | 在酸性条件下水解生成两种有机产物的相对分子质量可能相等 |
|
| D. | 在碱性条件下可完全水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:
①加入稍过量的Na2CO3溶液;
②加入稍过量的NaOH溶液;
③加入稍过量的BaCl2溶液;
④滴入稀盐酸至无气泡产生;
⑤过滤;
正确的操作顺序是()
A. ③②①⑤④ B. ①②③⑤④ C. ②③①⑤④ D. ③⑤②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
完成下列反应的离子方程式
(1)硫酸氢钠溶液中加入硝酸钡溶液产生白色沉淀: ;
(2)在小苏打(NaHCO3)溶液中加盐酸,有无色气体产生: ;
(3)在200mL的烧杯中加入50mL蒸馏水,加热至沸腾,滴入10滴饱和氯化铁溶液,继续加热至溶液呈红褐色 .
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A. NH4+、Ba2+、Br﹣、CO32﹣ B. Cl﹣、SO32﹣、Fe2+、H+
C. K+、Na+、SO42﹣、MnO4﹣ D. Na+、H+、NO3﹣、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中的离子能在溶液中大量共存的是( )
A. K+、NH4+、SO42﹣、OH﹣ B. Na+、Ca2+、CO32﹣、NO3﹣
C. Na+、H+、Cl﹣、HCO3﹣ D. Na+、Cu2+、Cl﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
北京奥运会期间对大量盆栽鲜花施用了S﹣诱抗素制剂,以保持鲜花盛开.S﹣诱抗素的分子结构如图,下列关于该分子说法正确的是()
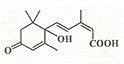
A. 含有碳碳双键、羟基、碳基、羧基
B. 1mol该物质可消耗2molNaOH
C. 分子式为C14H20O4
D. 1mol该物质可与4molH2加成
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释事实的方程式不正确的是()
A. 测0.1mol/L氨水的pH为11:NH3•H2O⇌NH4++OH﹣
B. 将Na块放入水中,产生气体:2Na+2H2O═2NaOH+H2↑
C. 用CuCl2溶液做导电实验,灯泡发光:CuCl2 Cu2++2Cl﹣
Cu2++2Cl﹣
D. Al片溶于NaOH溶液中,产生气体:2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com