
【题目】如图所示,从A处通入Cl2。当关闭B阀时,C处的红布逐渐褪色;当打开B阀后,C处的红布无明显现象,则下列判断正确的是
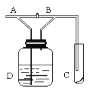
A.通入的Cl2可能是潮湿的B.红布一定是干燥的
C.D中的液体可能是NaOHD.使红布褪色的物质是Cl2
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:
元素 | 相关信息 |
A | 基态原子的价电子排布式为nSnnPn |
B | 元素原子的核外p电子数比s电子数少1个 |
C | 最外层电子数是电子层数的3倍 |
D | 简单离子是第三周期元素中离子半径最小的 |
E | 价电子层中的未成对电子数为4 |
请回答下列问题:
(1)写出下列元素符号:A______, B_______,C________,D__________。
(2)写出C元素在周期表的位置_________,E2+价电子的轨道表示式______________,B元素能量最高的电子为____轨道上的电子,其轨道呈______形。
(3)按原子轨道的重叠方式,1molA与C形成的最高价化合物中σ键有______个,π键有______个。(阿伏加德罗常数的值用NA表示)
(4)B、C、D的简单离子的半径由大到小的顺序为________(用离子符号表示)。
(5)写出C的核外有18个电子的氢化物的电子式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2与NaOH溶液反应可生成NaCl、NaClO和NaClO3(Cl-和ClO-)的比值与反应的温度有关,用24gNaOH配成的250mL溶液,与Cl2恰好完全反应(忽略Cl2与水的反应、盐类的水解及溶液体积变化):
(1)NaOH溶液的物质的量浓度_____mol·L-1;
(2)某温度下,反应后溶液中c(Cl-)=6c(ClO-),则溶液中c(ClO-) =_____mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在汽车尾气处理装置中加入适当的催化剂,能发生如下反应:4CO+2NO2![]() 4CO2+N2。下列对该反应的说法中错误的是
4CO2+N2。下列对该反应的说法中错误的是
A. 该反应是氧化还原反应
B. 该反应中氧化剂是CO、还原剂是NO2
C. 该反应生成28 g N2时,转移8 mol e-
D. 该反应将能减少汽车尾气对环境的污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,A、B、C、D、E、F、G均为有机化合物。
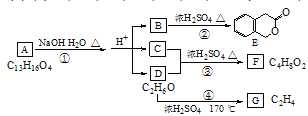
根据上图回答问题:
(1)D、F的化学名称是________、________。
(2)写出下列反应的化学方程式,并注明反应类型。
②____________________________________________,________;
④____________________________________________,________;
(3)A的结构简式是__________________,1 mol A与足量的NaOH溶液反应会消耗________mol NaOH。
(4)写出符合下列3个条件的B的同分异构体____________________。
①含有邻二取代苯环结构②与B有相同官能团③不与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铼熔点高、耐磨、耐腐蚀,广泛用于航天航空等领域。工业上用富铼渣(含ReS2)制得铼粉,其工艺流程如下图所示:
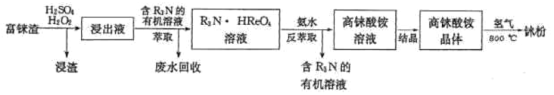
回答下列问题
(1)下图是矿样粒度与浸出率关系图,浸出时应将富铼渣粉碎至___________目;请给出提高铼浸出率的另外两种方法:___________。浸出反应中ReS2转化为两种强酸,请写出铼浸出反应的离子方程式:______________________。

(2)上图表示萃取液流速与铼吸附率关系。结合实际工业生产效益,萃取剂流速宜选用的范围是___________BV/h。
(3)已知高铼酸铵不溶于冷水,易溶于热水。提纯粗高铼酸铵固体的方法是___________。
(4)高铼酸铵热分解得到Re2O7,写出氢气在800℃时还原Re2O7制得铼粉的化学方程式______________________。
(5)整个工艺流程中可循环利用的物质有:H2SO4、___________、___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关说法正确的是
A. 0.2L 3mol·L-1的NH4Cl溶液与0.3L2mol·L-1的NH4Cl溶液中NH4+的数目均为0.6NA
B. 标准状况下,11.2L乙烯和环丙烷的混合气体中,共用电子对的数目为3NA
C. 常温下,1LpH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA
D. ag某气体所含分子数为b个,则cg该气体的体积为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四种X溶液,均能跟盐酸反应,其中反应最快的是( )
A. 10 ℃ 3 mol·L-1的X溶液
B. 20 ℃ 3 mol·L-1的X溶液
C. 10 ℃ 2 mol·L-1的X溶液
D. 20 ℃ 2 mol·L-1的X溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com