
 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.分析 (1)根据金属活动性顺序表可以判断钠、钾、镁、铝的活泼性,活泼性越强,与盐酸反应越剧烈;根据电子守恒比较生成氢气体积大小;
(2)硫离子被氯气氧化成硫单质,据此写出反应的离子方程式;
(3)元素的最高价氧化物的水化物的碱性越强,元素的金属性越强;
(4)根据仪器的构造写出仪器B的名称;球形干燥管具有防止倒吸的作用;
(5)氯气能够将碘离子氧化成碘单质,碘单质遇到淀粉变成蓝色;氯气有毒,氯气能够与氢氧化钠溶液反应;
(6)碳酸酸性强于硅酸,二氧化碳能够与硅酸钠反应生成白色沉淀硅酸;除去二氧化碳中氯化氢,可以使用饱和碳酸氢钠溶液.
解答 解:Ⅰ(1)金属活泼性顺序为:钾>钠>镁>铝,所以相同条件下与盐酸反应最激烈的是钾,反应速率最慢的是铝;生成1mol氢气需要得到2mol电子,1mol钾、钠都失去1mol电子,1mol镁失去2mol电子,而1mol铝失去3mol电子,所以生成氢气最多的是金属铝,
故答案为:钾;铝;铝;
(2)氯气氧化性强于硫单质,所以氯气能够与硫离子反应生成硫,反应的离子方程式为:S2-+Cl2═S↓+2Cl-,
故答案为:S2-+Cl2═S↓+2Cl-;
(3)将NaOH溶液与NH4Cl溶液混合生成NH3•H2O,可以说明NaOH的碱性大于NH3•H2O,但不能说明Na的金属性大于N,因为要验证金属性的强弱,必须通过比较最高价氧化物所对应的水化物的碱性来进行比较,而NH3•H2O不是氮元素的最高价氧化物的水化物,
故答案为:不合理,用碱性强弱比较金属性强弱时,一定要用元素的最高价氧化物的水化物的碱性强弱比较,而NH3•H2O不是氮元素的最高价氧化物的水化物.
Ⅱ(4)仪器B为锥形瓶;球形干燥管D能够防止倒吸,可以避免C中液体进入锥形瓶中,
故答案为:锥形瓶;倒吸;
(5)KMnO4与浓盐酸常温下反应生成氯气,氯气能够将碘离子氧化成碘单质,碘单质遇到淀粉变成蓝色,氯气是一种有毒气体,必须进行尾气吸收,氯气能够与氢氧化钠溶液反应,可以使用氢氧化钠溶液吸收多余的氯气,
故答案为:变蓝;NaOH;
(6)氯化氢具有挥发性,干扰实验结果,需要将二氧化碳中的氯化氢除掉,根据氯化氢与碳酸氢钠反应,而二氧化碳不反应,可以在B和C之间增加装有饱和NaHCO3溶液的洗气瓶,
故答案为:有白色沉淀生成;饱和NaHCO3.
点评 本题考查了探究金属单质的金属性强弱、非金属单质的非金属性强弱方法,题目难度中等,正确掌握判断金属性、非金属性强弱的方法,明确除杂试剂的作用原则:除去装置,不能引进新的杂质.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑ | B. | MgCO3+CO2+H2O═Mg(HCO3)2 | ||
| C. | MgCO3+H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑ | D. | CaCO3+H2O═Ca(OH)2+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.lmol•L-lNaHC2O4溶液(pH=5.5):c(Na+)>c( HC2O4-)>c(H2C2O4)>c(C2O42- ) | |
| B. | 0.lmol•L-1NaHS 溶液:C(OH-)+c(S2-)=c( H+)+c(H2S) | |
| C. | 0.lmol•L-1CH3COOH 溶液和 0.lmol•L-1CH3COONa 溶液等体积混合:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c( OH-) | |
| D. | 0.lmol•L-lNH4HSO4 溶液中滴加 0.lmol•L-1NaOH 溶液至中性:c(Na+ )>c(SO42- )>c(NH4+ )>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
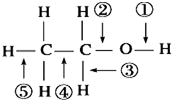
| A. | 乙醇与钠反应,键①断裂 | |
| B. | 乙醇在Ag催化作用下与O2反应,键①③断裂 | |
| C. | 乙醇完全燃烧时,只有①②键断裂 | |
| D. | 乙醇与氢卤酸反应,键②断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
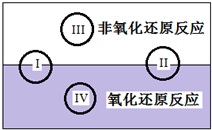 氧化还原反应在生产、生活中具有广泛的用途.请回答下列问题:
氧化还原反应在生产、生活中具有广泛的用途.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来,金属铝的熔点较低 | |
| B. | 铝与Fe2O3发生铝热反应后固体的质量不变 | |
| C. | Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | Al、HCl、NaOH中任意两种物质在一定条件下均能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠溶液 | B. | 氨水 | C. | 硝酸银溶液 | D. | 氯化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18.4mol•L-1 34.7% | B. | 20.4mol•L-1 38.5% | ||
| C. | 18.4mol•L-1 38.5% | D. | 20.4mol•L-1 34.7% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com