
弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
Ⅰ.已知H2A在水中存在以下平衡:H2A===H++HA-,HA-H++A2-。
(1)常温下NaHA溶液的pH________(填选项字母),原因是________。
A.大于7 B.小于7
C.等于7 D.无法确定
(2)某温度下,若向0.1 mol·L-1的NaHA溶液中逐滴滴加0.1 mol·L-1 KOH溶液至溶液呈中性(忽略混合后溶液的体积变化)。此时该混合溶液中的下列关系一定正确的是________。
A.c(H+)·c(OH-)= 1.0×10-14
1.0×10-14
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)=0.05 mol·L-1
(3)已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s)Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有________(填选项字母)。
A.升高温度 B.降低温度
C.加入NH4Cl晶体 D.加入Na2A固体
Ⅱ.含有Cr2O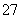 的废水毒性较大,某工厂废水中含5.0×10-3 mol·L-1的Cr2O
的废水毒性较大,某工厂废水中含5.0×10-3 mol·L-1的Cr2O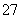 。为了使废
。为了使废 水的排放达标,进行如下处理:
水的排放达标,进行如下处理:
Cr2O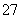
 Cr3+、Fe3+
Cr3+、Fe3+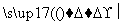 Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3
(1)该废水中加入绿矾和H+,发生反应的离子方程式为___________。
(2)若处理后的废水中残留的c(Fe3+)=2.0×10-13 mol·L-1,则残留的Cr3+的浓度为______________。(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH) 3]=6.0×10-31)
3]=6.0×10-31)
解析 H2A在水中的一级电离进行完全,则HA-不水解只电离,故NaHA溶液呈酸性。HA-在水中部分电离,0.1 mol·L-1的NaHA溶液中c(H+)小于0.1 mol·L-1,加入0.1 mol·L-1 KOH溶液至溶液呈中性时消耗的KOH溶液体积小于NaHA溶液体积,则混合溶液中c(Na+)>c(K+);由电荷守恒知,c(Na+)+c(K+)+c(H+)=c(HA-)+2c(A2-)+c(OH-),且c(H+)=c(OH-),则c(Na+)+c(K+)=c(HA-)+2c(A2-);水的离子积与温度有关;c(Na+)+c(K+)=0.1 mol·L-1。降温、增大c(A2-)都能使平衡CaA(s)Ca2+(aq)+A2-(aq)左移。废水中加入绿矾和H+ ,根据流程图,可知发生的是氧化还原反应,配平即可。c(Cr3+)/c(Fe3+)=[c(Cr3+)·c3(OH-)]/[c(Fe3+)·c3(OH-)]=Ksp[Cr(OH)3]/Ksp[Fe(OH)3]=1.5×107,故c(Cr3+)=3.0×10-6 mol·L-1。
,根据流程图,可知发生的是氧化还原反应,配平即可。c(Cr3+)/c(Fe3+)=[c(Cr3+)·c3(OH-)]/[c(Fe3+)·c3(OH-)]=Ksp[Cr(OH)3]/Ksp[Fe(OH)3]=1.5×107,故c(Cr3+)=3.0×10-6 mol·L-1。
答案 Ⅰ.(1)B NaHA只能发生电离,不能发生水解
(2)BC
(3)BD
Ⅱ.(1)Cr2O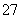 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
(2)3.0×10-6 mol·L-1


科目:高中化学 来源: 题型:
目前国内外使用的融雪剂一般有两大类:一类是以醋酸钾为主要成分的有机融雪剂;另一类是以“氯盐”为主要成分的无机融雪剂,如氯化钠、氯化钙、氯化镁等,通称“化冰盐”。某研究性学习小组拟对融雪氯盐(主要含有氯化钠及不溶性杂质、Mg2+、Ca2+等)进行回收提纯研究。
| 化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
| Ksp | 2.8×10-9 | 6.8×10-8 | 4.0×10-9 | 1.8×10-11 |
该小组设计流程如图:

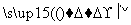
(1)加入混合液A的主要成分是________________(填化学式)。
(2)为检验溶液B中的Mg2+、Ca2+,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+,向其中一支试管中加入________溶液(填化学式),看是否有沉淀生成。
步骤二:检验Ca2+,向另一支试管中加入某溶液,看是否有沉淀生成。下列三种溶液,其沉淀效果最好的是________。
A.0.1mol·L-1 Na2CO3溶液
B.0.1mol·L-1 Na2SO3溶液
C.0.1mol·L-1 Na2C2O4溶液
(3)在除杂过程中,向粗盐悬浊液中加混合液A时需控制溶液pH=12以确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在________________以下。
(4)对溶液B加热并不断滴加6mol·L-1的盐酸,同时用pH试纸检测溶液,直至pH=2时停止加盐酸,得到溶液C。该操作的目的是__________________________________________________。
(5)溶液C倒入蒸发皿中,加热蒸发并用玻璃棒不断搅拌,直到有大量固体析出时停止加热。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作过程能引起实验结果偏高的是( )
①用已知浓度的盐酸滴定未知浓度的NaOH溶液时,酸式滴定管未用标准液润洗
②用量筒量取5.0 mL溶液时,俯视读数
③配制一定物质的量浓度的硫酸溶液,定容时仰视容量瓶的刻度线
④质量分数为10%和90%的两种硫酸等体积混合配制50%的硫酸溶液
A.①③ B.①④
C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,向2 L恒容密闭容器中充入1.0 mol A和1.0 mol B,反应A(g)+B(g)C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A.反应在前5 s的平均速度v(A)=0.17 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(A)=0.41 mol·L-1,则反应的ΔH>0
C.相同温度下,起始时向容器中充入2.0 mol C,达到平衡时,C的转化率大于80%
D.相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,反应达到平衡前v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
有0.1mol·L-1的三种溶液:①CH3COOH ②NaOH ③CH3COONa,下列说法正确的是( )
A.溶液①中,c(CH3COO-)=c(H+)
B.溶液①②等体积混合,混合液中c(CH3COO-)等于溶液③中的c(CH3COO-)
C.溶液①②等体积混合,混合液中c(CH3COO-)+c(CH3COOH)=c(Na+)
D.溶液①③等体积混合,混合液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象不能说明相关结论的是( )
A.将铜与浓硫酸共热,产生 使石蕊溶液变红的气体,说明浓硫酸具有酸性
使石蕊溶液变红的气体,说明浓硫酸具有酸性
B.将金属钠投入冷水中,钠熔为小球,说明钠与水的反应为放热反应且钠的熔点低
C.向AgCl浊液中滴加Na2S溶液,白色沉淀变成黑色,说明AgCl的溶解平衡正向移动
D.向Al(OH)3沉淀中滴加NaOH溶液或盐酸,沉淀均消失,说明Al(OH)3是两性氢氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
用FeCl3酸性溶液脱除H2S后的溶液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1 mol/L FeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压值):
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(1)用KSCN溶液检验出Fe3+的现象是___________________。
(2)Ⅰ中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应的方程式:__________________________________。
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有________性。
(4)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
①NaCl溶液的浓度是________mol/L。
②Ⅳ中检验Cl2的实验方法___________________________。
③与Ⅱ对比,得出的结论(写出两点)___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,有下列三个热化学方程式:
(1)2H2(l)+O2(g)=== 2H2O(l) △H1= -Q1 kJ• mol-1
(2)2H2(g)+O2(g)=== 2H2O(l) △H1= -Q2 kJ• mol-1
(3)2H2(l)+O2(g)=== 2H2O(g) △H1= -Q3 kJ• mol-1
则Q1、Q2、Q3的关系表示正确的是( )
A. Q1=Q2<Q3 B. Q2 > Q1 >Q3 C. Q3> Q2> Q1 D. Q1=Q2=Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
欲用98%的浓硫酸(p=1.84g·cm-3 )配制成浓度为0.5mol·L-1的稀硫酸500ml。
(1) 选用的主要仪器有:
①__________,②__________,③__________,④____________,⑤____________。
(2) 请将下列各操作,按正确的序号填在横线上。
A.用量筒量取浓H2SO4 B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线 D.洗净所用仪器
E.稀释浓H2SO4 F.将溶液转入容量瓶
其操作正确的顺序依次为__________ __________________。
(3)简要回答下列问题:
①所需浓硫酸的体积为____________mL。
(4)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了______________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com