

���� ��1�����ݴ�����������ʣ���ˮϡ�������ڵ���ƽ�������ƶ�����������ǿ����ʣ������ڵ���ƽ�⣻
��2����Kw�Ĵ�Сֻ���¶�Ӱ�죻��Һ������Ũ��Խ������Խǿ��
��Ka�Ĵ�Сֻ���¶�Ӱ�죬�¶Ȳ������С���䣬��������ƣ����������Ũ������
��3������Ϊ���ᣬpH��Ϊ2������ʹ�����Һ��������Һ��H+����Ũ����ȣ������Ũ�ȴ������ᣬ�ֱ��к͵�����������ʵ���Ũ�ȵ�����������Һ������������ǡ�ñ���ȫ�к�ʱ�����ĵ�����������ʵ�����ȣ�����n=C��V�Ƚ϶��ߵ������ϵ��
��4�����ܵ���ʵ��ܽ�ƽ�⼰����ת�����ܽ�ȴ���������ܽ��С������ת����
��5����Ka�Ĵ�С�ж�������ǿ����Ҫ��������ǿ�������Բ��ö��ַ�������������ˮ��ԭ������Խ����Ӧ��ǿ���ξ�Խ��ˮ�⣩��Ҳ�������ý�ǿ������ȡ�������������飮
��� �⣺��1����Ϊ���������ᣬ��ˮ��Ӧ������У������������ӣ���ˮ��������Ũ���ڼ�С�Ĺ���������������ƣ���������ǿ����ˮ����ȫ���룬��ˮ��������Ũ��ֻ���ڼ�С������Ҫʹϡ�ͺ�����ҺpHֵ��ͬ���ͱ���ʹm��n���ʴ�Ϊ������
��2����Kw�Ĵ�Сֻ���¶�Ӱ�죬��ͬ�¶��£�Kw��a��=Kw��c�����ڴ�����Һ��������Һ�У�pHԽС������Ũ��Խ����Һ��������Խǿ���ʴ�Ϊ��=��a��b��c��
��Ka�Ĵ�Сֻ���¶�Ӱ�죬�¶Ȳ������С���䣬��������ƣ����������Ũ����������$\frac{c��{H}^{+}��}{c��C{H}_{3}COOH��}$�ı�ֵ��С���ʴ�Ϊ����С��
��3������Ϊ���ᣬpH��Ϊ2������ʹ�����Һ��������Һ��H+����Ũ����ȣ������Ũ�ȴ������ᣬ�������Ũ��ΪC1�������Ũ��ΪC2����C1��C2���ֱ��к���������ʱ���������ĵ��������Ƶ����ʵ����������ᣬ�ʴ�Ϊ������
��4�����ܵ���ʵ��ܽ�ƽ�⼰����ת�����ܽ�ȴ���������ܽ��С������ת����ZnS��PbS��ת��ΪCuS������CuS���ܽ��С��ZnS��PbS���ܽ�ȣ�
�ʴ�Ϊ��CuS���ܽ��С��ZnS��PbS���ܽ�ȣ�
��5��H2SO3�ĵ��볣��Ka2��=6.3��10-8��H2CO3�ĵ��볣��Ka1=4.2��10-7�����Ե����ʵ���Ũ�ȵ�NaHSO3��H2CO3��Һ�����Խ�ǿ����̼�Ҫ��������ǿ�������Բ��ö��ַ�������������ˮ��ԭ������Խ����Ӧ��ǿ���ξ�Խ��ˮ�⣩��Ҳ�������ý�ǿ������ȡ�������������飬���ֲο��������£�
����һ��������ͬ���ʵ���Ũ�ȵ�NaHSO3��NaHCO3��Һ������ȼƣ���pH��ֽ��������Һ��pH��ǰ�ߵ�pHС�ں��ߣ�֤��H2SO3����ǿ��H2CO3��
����������SO2��������ͨ��NaHCO3��Na2CO3����Һ������KMnO4��Һ��Ʒ����Һ������ʯ��ˮ��Ʒ����Һ����ɫ���ҳ���ʯ��ˮ����ǣ�֤��H2SO3����ǿ��H2CO3��
����������CO2��������ͨ��NaHSO3��Na2SO3����Һ��Ʒ����Һ��Ʒ����Һ����ɫ��֤��H2SO3����ǿ��H2CO3��
�ʴ�Ϊ��̼�����һ��������ͬ���ʵ���Ũ�ȵ�NaHSO3��NaHCO3��Һ������ȼƣ���pH��ֽ��������Һ��pH��ǰ�ߵ�pHС�ں��ߣ�֤��H2SO3����ǿ��H2CO3��
����������SO2��������ͨ��NaHCO3��Na2CO3����Һ������KMnO4��Һ��Ʒ����Һ������ʯ��ˮ��Ʒ����Һ����ɫ���ҳ���ʯ��ˮ����ǣ�֤��H2SO3����ǿ��H2CO3��
����������CO2��������ͨ��NaHSO3��Na2SO3����Һ��Ʒ����Һ��Ʒ����Һ����ɫ��֤��H2SO3����ǿ��H2CO3��
���� ������Ҫ����ˮ�����ӻ�������������ʵĵ��볣��ֻ���¶�Ӱ�졢�����Ļ���ʵ�������������ʹ�á����ӵij��Ӻ�ʵ�鷽����ƣ��ۺ���ǿ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ȶ��ԣ�HF��HCl��HBr��HI | B�� | ���ԣ�HClO4��H2SO4��H3PO4 | ||
| C�� | ���Ӱ뾶��N3-��O2-��F-��Na+��Mg2+ | D�� | �е㣺F2��Cl2��Br2��I2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͼ��A��B��C���ֹ������ʵ��ܽ������ͼ����ش�
��ͼ��A��B��C���ֹ������ʵ��ܽ������ͼ����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0•12mol | B�� | 0•08mol | C�� | 0•04mol | D�� | 0•8mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������뻹ԭ�������ʵ���֮��Ϊ1��5 | |
| B�� | �ù���˵��KMnO4�ữʱ���ܵμ����� | |
| C�� | ��Ӧ������ת��2mol����ʱ������Cl2�����ԼΪ22.4L | |
| D�� | ���Ѹ÷�Ӧ��Ƴ�ԭ��أ���������ӦΪMnO4-+5e-+8H+�TMn2++4H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

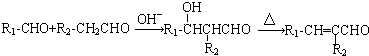
 ����Ӧ�١���������ȡ����Ӧ���Тۢܢݣ�����ţ���
����Ӧ�١���������ȡ����Ӧ���Тۢܢݣ�����ţ��� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2CO3�� | B�� | NaHC03 | C�� | K2CO3 | D�� | CaCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 60 g SiO2�����к���Si-O����ĿΪ2NA | |
| B�� | ���³�ѹ�£�1.6 9 O2��O3�Ļ����������������Ϊ0.8NA | |
| C�� | 1 mol/L AICl3��Һ�У�����Al3+��ĿС��NA | |
| D�� | �ܱ�������2 mol NO��l mol 02��ַ�Ӧ������ķ�����Ϊ2NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com