
【题目】将 ![]() 转变为
转变为 ![]() 的方法为( )
的方法为( )
A.溶液加热,通入足量的HCl
B.与足量的NaOH溶液共热后,再通入CO2
C.与稀H2SO4共热后,加入足量的Na2CO3
D.与稀H2SO4共热后,加入足量的NaOH
【答案】B
【解析】解:A.溶液加热并通入足量HCl,酯基和﹣COONa都反应,应该生成﹣OH、﹣COOH,故A错误;
B.加入NaOH溶液并加热,酯基和NaOH反应生成酚钠,然后再通入二氧化碳,生成﹣OH,故B正确;
C.和稀硫酸混合,﹣COONa、酯基都反应分别生成﹣COOH、﹣OH,然后加入足量的碳酸钠,碳酸钠和酚羟基、羧基都反应,故C错误;
D.和稀硫酸反混合,﹣COONa、酯基都反应分别生成﹣COOH、﹣OH,然后加入足量NaOH,羧基和酚羟基都和NaOH反应,故D错误;
故选B.
将 ![]() 转变为
转变为 ![]() ,﹣COONa不变,则先发生碱性条件下水解,再将酚钠转化为酚﹣OH,以此来解答.
,﹣COONa不变,则先发生碱性条件下水解,再将酚钠转化为酚﹣OH,以此来解答.


科目:高中化学 来源: 题型:
【题目】早期发现的一种天然准晶颗粒由Al、Cu、Fe三种元素组成.回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过方法区分晶体、准晶体和非晶体.
(2)基态铁原子有_个未成对电子,三价铁离子的电子排布式为 . 三价铁离子比二价铁离子的稳定性更好,原因是 .
(3)新制备的氢氧化铜可将乙醛氧化为乙酸,而自身还原成氧化亚铜,乙醛中碳原子的杂化轨道类型为;乙酸的沸点明显高于乙醛,其主要原因是 .
(4)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2﹣ , 在形成配位键时,弧对电子由元素提供.
(5)氧化亚铜为半导体材料,在其立方晶胞内部有四个氧原子,其余氧原子位于面心和顶点,则该晶胞中有个铜原子.
(6)铝单质为面心立方晶体,其晶胞边长a=0.405nm,晶胞中铝原子的配位数为 . 列式表示铝单质的密度gcm﹣3(不必计算出结果).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于1mol·L-1的Na2SO4溶液说法正确的是( )
A. 溶液中含有1molNa2SO4 B. 1mol Na2SO4溶于1L水中制得
C. 1L溶液中含有1 mol Na2SO4 D. Na+的浓度是1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 的系统命名为2﹣甲基﹣2﹣乙基丙烷
的系统命名为2﹣甲基﹣2﹣乙基丙烷
B.用酸性KMnO4溶液可以确定CH2=CH﹣CHO中含有C=C双键
C.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
D.在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为实现消除碘缺乏病的目标,卫生部规定食盐必须加碘,其中的碘以碘酸钾(KIO3)形式存在.已知在溶液中IO3-可以和I-发生反应: IO3-+5I-+6H+===3I2+3H2O,根据此反应,可用试纸和生活中常见的一些物质进行实验,证明在食盐中存在IO3-.进行上述实验时必须使用的物质是( )
①自来水 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④淀粉 ⑤食糖 ⑥食醋 ⑦白酒
A.①③
B.③⑥
C.②④⑥
D.①②④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁溶液与氢氧化铁胶体具有的共同性质是
A. 分散质颗粒直径都在l~100nm 之间 B. 能透过半透膜
C. 加入浓氢氧化钠溶液都产生红褐色沉淀 D. 颜色都呈红褐色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知维生素A1的键线式如下,线的交点与端点处代表碳原子,并用氢原子补足四价,但C、H原子未标记出来.
请回答下列问题:
(1)维生素A中的含有官能团种类有 , (官能团名称),它使溴水褪色(填“能”或“否”),
(2)维生素A1的结构简式如图,若1mol维生素A1分子最多可跟molH2发生加成反应. 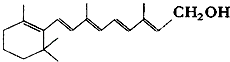
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com