
【题目】在密闭容器中进行如下反应:X2(g)+Y2(g)![]() 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下当反应达到平衡时,各物质的浓度有可能是( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下当反应达到平衡时,各物质的浓度有可能是( )
A.Z为0.3mol/LB.Y2为0.45mol/L
C.X2为0.2mol/LD.Z为0.4mol/L
【答案】A
【解析】
Z全部转化时,X2的物质的量浓度为:0.1+0.2÷2=0.2molL1,Y2的物质的量浓度为:0.3+0.2÷2=0.4molL1,故c(X2)的取值范围为:0<c(X2)<0.2molL1;当X2全部转化时,Z的物质的量浓度为:0.2+0.1×2=0.4molL1,Y2的物质的量浓度为:0.30.1=0.2molL1,故c(Y2)的取值范围为:0.2molL1<c(Y2)<0.4molL1,c(Z)的取值范围为:0<c(Z)<0.4molL1。
A. c(Z)的取值范围为:0<c(Z)<0.4molL1,Z为0.3mol/L有可能,故A正确;
B. c(Y2)的取值范围为:0.2molL1<c(Y2)<0.4molL1,Y2为0.45mol/L不可能,故B错误;
C. c(X2)的取值范围为:0<c(X2)<0.2molL1,所以X2为0.2mol/L不可能,故C错误;
D. c(Z)的取值范围为:0<c(Z)<0.4molL1;所以Z不可能为0.4mol/L,故D错误,
故选:A。


科目:高中化学 来源: 题型:
【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定,下列实验中用高锰酸钾与浓盐酸反应制备得到氯气,然后再将氯气通入氢氧化钾溶液中与氢氧化铁固体充分反应而制得产品:
(1)制备K2FeO4(夹持装置略)
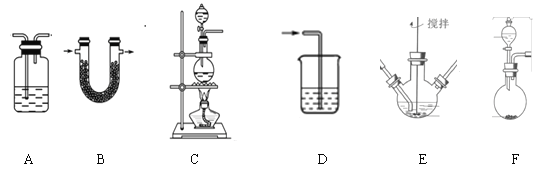
①请写出该过程中制备氯气的离子反应方程式________________(锰被还原为Mn2+)。
②请根据高铁酸钾制备的原理选择合适的装置,连接顺序为_________→ E →_________。(上述装置不一定全部用到,装置可以重复选用)
③装置E中反应时需进行搅拌,目的是_______________________
④E中得到紫色固体和溶液。E中生成高铁酸钾的反应为______________;反应充分进行后,E中溶液中主要的阴离子为__________________
(2)探究K2FeO4的性质
取E中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否是K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤E中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
①由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________产生(用方程式表示)。
②方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种集氧化、杀菌、脱色、除臭的新型高效水处理剂,工业上可通过 Fe(NO3)3 与NaClO在强碱性介质中反应生成紫红色高铁酸盐溶液,其对应的工业流程如图所示。有关说法正确的是( )
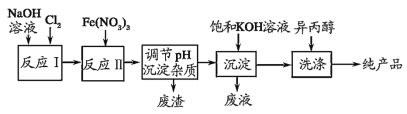
A.K2FeO4能够作为净水剂的原因,在于其氧化产物能够水解生成氢氧化铁胶体
B.反应II的离子方程式为 3ClO+5H2O+2Fe3+=2![]() +3Cl+10H+
+3Cl+10H+
C.向Na2FeO4 中加入饱和KOH 溶液,析出K2FeO4 沉淀,说明K2FeO4 的溶解度比Na2FeO4 大
D.洗涤粗品时选用异丙醇而不用水,可以减少K2FeO4的溶解损失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于密闭容器中的反应:2SO2(g)+O2(g)![]() 2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是
2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是

A.点c处反应达到平衡
B.点a的正反应速率比点b的大
C.点d (t1时刻)和点e (t2时刻)处n(SO2)不一样
D.其他条件不变,600℃时反应至t1时刻,n(SO 3)比上图中的e点值要大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在定温定容的密闭容器中合成 ![]() 。下列不能说明反应
。下列不能说明反应 ![]() 达到化学平衡状态的是
达到化学平衡状态的是
A.![]() B.容器内的压强不再改变
B.容器内的压强不再改变
C.![]() 的生成速率与
的生成速率与 ![]() 的消耗速率相等D.
的消耗速率相等D.![]() 的转化率不再改变
的转化率不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2 mol SO2和2 mol SO3气体混合于某固定体积的密闭容器中,在一定条件下反应:2SO2(g)+O2(g)![]() 2SO3(g),平衡时SO3为W mol。相同温度下,分别按下列配比在相同体积的容器中反应,反应达到平衡时,SO3的物质的量大于W mol的是( )
2SO3(g),平衡时SO3为W mol。相同温度下,分别按下列配比在相同体积的容器中反应,反应达到平衡时,SO3的物质的量大于W mol的是( )
A.2 mol SO2+1 mol O2B.4 mol SO2+1 mol O2
C.2 mol SO2+1 mol O2+2 mol SO3D.3 mol SO2+1 mol SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度下,有两种较稀的醋酸溶液A和B。A溶液中c(CH3COOH)=a mol·L-1,电离度为α1,B溶液中c(CH3COO-)=a mol·L-1,电离度为α2。下列叙述中正确的是( )
A.B溶液中c(CH3COOH)= ![]() mol·L-1
mol·L-1
B.A溶液的pH值小于B溶液的pH值
C.α2>α1
D.A溶液的c(H+)是B溶液c(H+)的0.5α1倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在当今社会,氮的氢化物和氧化物与我们的生活息息相关.
(1)NO是一种污染物,工业上用NH3、O2脱除烟气中NO的原理如图所示,该原理中NO最终转化为______(填化学式),V4+﹣O﹣H在反应过程中作___________。当消耗2molNH3和0.5molO2时,除去的NO在标准状况下的体积为____________L。

(2)N2H4是发射航天火箭的常用燃料,已知:N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=﹣538kJ·mol﹣1。断开1mol下列化学键系数的能量分别为N﹣H:390kJ、N≡N:946kJ、O﹣H:460kJ、O=O:498kJ。则断开1molN﹣N需要吸收的能量是__________.
(3)工业制硝酸时,会发生反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H<0。
4NO(g)+6H2O(g) △H<0。
①若其它条件不变,则下列图象不正确的是_____(填字母)。
A. B.
B.  C.
C. D.
D.
②在1L容积固定的密闭容器中充入NH3和O2发生该反应,部分物质的浓度随时间的变化如下表所示。
| c(NH3)/mol·L﹣1 | c(O2)/mol·L﹣1 | c(NO)mol·L﹣1 |
0 | 1.2 | 1.75 | 0 |
4min | 0.4 | 0.75 | 0.8 |
6min | 0.4 | 0.75 | 0.8 |
8min | 0.6 | 1 | 0.6 |
9min | 0.6 | 1 | 0.6 |
10min | 1.05 | 1 | 1.05 |
12min | … | … | … |
0~4min内,用O2表示该反应的平均反应速率为______mol·L﹣1·min﹣1。反应6~8min时改变了反应条件,改变的反应条件可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成问题
![]() 通过如图所示电解装置可将
通过如图所示电解装置可将![]() 转化为硫酸,电极材料皆为石墨。则A为电解池的_________
转化为硫酸,电极材料皆为石墨。则A为电解池的_________![]() 填“阴极”或“阳极”
填“阴极”或“阳极”![]() 。C为________
。C为________![]() 填物质名称
填物质名称![]() 。若将阴离子交换膜换成阳离子交换膜,写出阳极区域发生的电极反应:_______。
。若将阴离子交换膜换成阳离子交换膜,写出阳极区域发生的电极反应:_______。

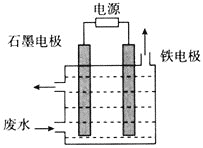
![]() 用如图所示装置处理含
用如图所示装置处理含![]() 废水时,控制溶液pH为
废水时,控制溶液pH为![]() 并加入NaCl,一定条件下电解,阳极产生的
并加入NaCl,一定条件下电解,阳极产生的![]() 将
将![]() 氧化为无害物质而除去。铁电极为_________
氧化为无害物质而除去。铁电极为_________![]() 填“阴极”或“阳极”
填“阴极”或“阳极”![]() ,阳极产生
,阳极产生![]() 的电极反应为_______,阳极产生的
的电极反应为_______,阳极产生的![]() 将
将![]() 氧化为无害物质而除去的离子方程式为______。
氧化为无害物质而除去的离子方程式为______。
![]() 以连二亚硫酸根离子
以连二亚硫酸根离子![]() 为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:

阴极区的电极反应式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com