
分析 把电子层数相同的各种元素按原子序数递增的顺序从左至右排成横行称为周期,把最外层电子数相同的元素按电子层数递增的顺序由上到下排列成纵行称为族,元素周期表共有18个纵行,16个族,七个周期,周期表中1、2、3为短周期,4、5、6为长周期,第7周期为不完全周期.
解答 解:元素周期表有七个横行共有七个周期,其中1、2、3周期称为短周期,4、5、6、7周期称为 长周期,其中第七周期尚未填满,又可称作不完全周期.元素周期表中共有 18个纵列,其中第8、9、10三个纵列称为第Ⅷ族,第18纵列由稀有气体元素组成,稀有气体元素的化学性质不活泼,化合价通常为0,因而这一族称为0族元素;其余14个纵列,每个纵列为 一个族,有 7个主族和7个副族之分,其中由短周期和 长周期共同组成的族称主族,符号为A,序数用罗马数字表示,仅由 长周期组成的族称为副族,符号为 B,序数用罗马数字表示,IB和ⅡB分别处在第11和第 12纵行.故答案为:七;短周期;长周期;七;18 第Ⅷ族; 0;0族元素;一个族;7个主族;7个副族;短; 长; A; 长;B;11; 12.
点评 本题考查了元素周期表的结构,题目难度不大,侧重于基础知识的考查,注意把握周期和族的编排依据.


科目:高中化学 来源: 题型:解答题
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
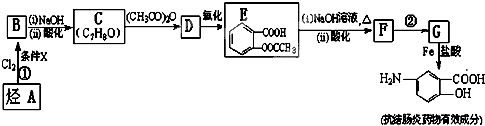
 .
. .
.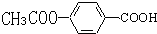
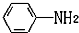 易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此写出以A为原料合成化合物
易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此写出以A为原料合成化合物 的合成路线
的合成路线 .(仿照题中抗结肠炎药物有效成分的合成路线的表达方式答题)
.(仿照题中抗结肠炎药物有效成分的合成路线的表达方式答题)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2通入高锰酸钾酸性溶液中,红色褪去 | |
| B. | SO2通入品红溶液中,红色褪去 | |
| C. | SO2通入溴水溶液中,红棕色褪去 | |
| D. | SO2通入氢氧化钠与酚酞的混合溶液中,红色褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HS-+H2O?H3O++S2- | B. | HS-+H2O?H2S+OH- | ||
| C. | HS-+H2O+=H2S↑+H2O | D. | CO32-+H2O+CO2=2HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com