
将1.68g铁粉加入到30.0mL的1.00 mol·L-1MO2+溶液中,恰好完全反应,向溶液中滴加KSCN溶液,溶液颜色没有变化,则还原产物可能是
| A.M | B.M+ | C.M2+ | D.M3+ |
科目:高中化学 来源: 题型:单选题
在一定温度下,1 mol金属铜与足量某浓度的硝酸完全反应,生成NO2和NO的物质的量之比为1:3,则反应过程中转移的电子为
| A.2 mol | B.3 mol | C.4mol | D.5 mo1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据反应①2FeCl3+2KI=2FeCl2+2KCl+I2,②2FeCl2+Cl2=2FeCl3,判断下列物质的氧化性由强到弱的顺序中,正确的是
| A.Fe3+>Cl2>I2 | B.Cl2>I2>Fe3+ | C.I2>Cl2>Fe3+ | D.Cl2>Fe3+>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Cl2是纺织工业中常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O32-和Cl2反应的产物之一为SO42-。下列说法中,不正确的是
| A.该反应中氧化剂是Cl2 |
| B.根据该反应可判断还原性:S2O32- > Cl- |
| C.上述反应中,每生成l mol SO42-,转移4 mol电子 |
| D.SO2与氯气的漂白原理相同,所以也可以用SO2做纺织工业的漂白剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于反应3Br2+6NaOH=5NaBr+NaBrO3+3H2O,以下叙述正确的是
| A.Br2是氧化剂,NaOH是还原剂 |
| B.氧化产物与还原产物的物质的量的比为5∶1 |
| C.Br2既是氧化剂又是还原剂 |
| D.每生成1mol的NaBrO3转移6mol的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
工业上常利用反应 3Cl2 + 6KOH(热) → KClO3 + 5KCl + 3H2O 制取KClO3(混有KClO)。实
验室模拟上述制备:在含溶质14mol的KOH(aq,热)中通入一定量Cl2,充分反应后,测得
溶液中n(Cl-)=11mol;将此溶液低温蒸干,得到的固体中KClO3的物质的量可能为
| A.2.20 | B.2.33 | C.2.00 | D.0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:
Li2NH+H2 LiNH2+LiH,下列有关说法正确的是( )
LiNH2+LiH,下列有关说法正确的是( )
| A.Li2NH中N的化合价是-1 | B.该反应中H2既是氧化剂又是还原剂 |
| C.Li+和H-的离子半径相等 | D.此法储氢和钢瓶储氢的原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示,两圆圈相交的阴影部分表示圆圈内物质相互发生的反应,其中属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )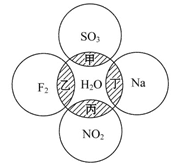
| A.甲 | B.乙 | C.丙 | D.丁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com