
| A£® | .µē³Ų¹¤×÷Ź±£¬MnO2·¢Éś»¹Ō·“Ó¦ | |
| B£® | .µē³Ųøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ2MnO2+H2O+2e-”śMn2O3+2OH- | |
| C£® | .µē³Ų¹¤×÷Ź±£¬µēĀ·ÖŠĆæĶعż0.2molµē×Ó£¬ŠæµÄÖŹĮæĄķĀŪÉĻ¼õÉŁ6.5g | |
| D£® | µē³Ų¹¤×÷Ź±£¬K+ŅĘĻņøŗ¼« |
·ÖĪö øł¾Żµē³Ų×Ü·“Ó¦Ź½ĪŖ£ŗZn£Øs£©+2MnO2£Øs£©+H2O£Øl£©ØTZn£ØOH£©2£Øs£©+Mn2O3£Øs£©£¬æÉÖŖ·“Ó¦ÖŠZn±»Ńõ»Æ£¬ĪŖŌµē³ŲµÄøŗ¼«£¬øŗ¼«·“Ó¦ĪŖZn-2e-+2OH-ØTZn£ØOH£©2£¬MnO2ĪŖŌµē³ŲµÄÕż¼«£¬·¢Éś»¹Ō·“Ó¦£¬Õż¼«·“Ó¦ĪŖ2MnO2£Øs£©+H2O£Ø1£©+2e-ØTMn2O3£Øs£©+2OH-£Øaq£©£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗA£®øł¾Ż×Ü·“Ó¦æÉÖŖ£¬MnO2ÖŠMnŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬·¢Éś»¹Ō·“Ó¦£¬¹ŹAÕżČ·£»
B£®øŗ¼«ZnŹ§µē×Ó£¬·¢ÉśŃõ»Æ·“Ó¦£¬ĖłŅŌøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗZn-2e-+2OH-=Zn£ØOH£©2£¬¹ŹB“ķĪó£»
C£®ÓÉZn£Øs£©+2MnO2£Øs£©+H2O£Øl£©ØTZn£ØOH£©2£Øs£©+Mn2O3£Øs£©æÉÖŖ£¬65gZn·“Ó¦×ŖŅʵē×ÓĪŖ2mol£¬Ōņ6.5gZn·“Ó¦×ŖŅĘ0.2molµē×Ó£¬¹ŹCÕżČ·£»
D£®µē³Ų¹¤×÷Ź±£¬µē×ÓÓÉøŗ¼«Į÷ĻņÕż¼«£¬øł¾ŻŅģŠŌµēŗÉĻąĪü£¬ČÜŅŗÖŠK+”¢H+ĻņÕż¼«ŅĘ¶Æ£¬OH-Ļņøŗ¼«ŅĘ¶Æ£¬¹ŹD“ķĪó£®
¹ŹŃ”AC£®
µćĘĄ ±¾Ģāæ¼²é»ÆѧµēŌ“µÄ¹¤×÷ŌĄķ£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢Ņāµē¼«·“Ó¦·½³ĢŹ½µÄŹéŠ“ŗĶŌµē³ŲÕżøŗ¼«µÄÅŠ¶Ļ£®Ąķ½āÕāĄąĢāµÄ¹Ų¼üŹĒĄķ½āŌµē³ŲŌĄķ£¬ŌŚ·“Ó¦ÖŠ£¬µē×Ó“Óøŗ¼«¾ĶāµēĀ·Į÷ĻņÕż¼«£¬Ķ¬Ź±ČÜŅŗÖŠµÄŅõ”¢ŃōĄė×Ó·Ö±š²»¶ĻŅĘĻņøŗ¼«”¢Õż¼«£¬¹¹³É±ÕŗĻ»ŲĀ·£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø | |
| B£® | 1 molŹÆÄ«Ėł¾ßÓŠµÄÄÜĮæ±Č1 mol½šøÕŹÆµĶ | |
| C£® | ½šøÕŹÆ×Ŗ±ä³ÉŹÆÄ«ŹĒĪļĄķ±ä»Æ | |
| D£® | ŹÆÄ«ŗĶ½šøÕŹÆ¶¼ŹĒĢ¼µÄĶ¬Ī»ĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | 1mol H2O ·Ö½āĪŖH2ÓėO2ŠčĪüŹÕ930 kJČČĮæ | |
| B£® | HÓėO·“Ӧɜ³É1mol H2O·Å³ö930 kJČČĮæ | |
| C£® | 2 mol HµÄÄÜĮæŠ”ÓŚ1mol H2µÄÄÜĮæ | |
| D£® | H½įŗĻ³ÉH2·Å³ö436 kJµÄČČĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øֻƲ£Į§ | B£® | ĘÆ°×·Ū | C£® | ĻūŹÆ»Ņ | D£® | Ė®²£Į§ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”°ŗ£Ė®µ»Æ”±æÉŅŌ½ā¾ö”°µĖ®¹©Ó¦Ī£»ś”±£¬Ļņŗ£Ė®ÖŠ¼ÓČė¾»Ė®¼ĮĆ÷·ÆæÉŅŌŹ¹ŗ£Ė®µ»Æ | |
| B£® | Ź³ÓĆÓĶŗĶČĖŌģÄĢÓĶ¶¼ŹĒÓĶĖįøŹÓĶõ„ | |
| C£® | Ö»ŅŖ·ūŗĻĻŽĮ棬”°Ź³ÓĆÉ«ĖŲ”±”¢”°ŃĒĻõĖįŃĪ”±æÉŅŌ×÷ĪŖijŠ©Ź³Ę·µÄĢķ¼Ó¼Į | |
| D£® | ¼¦µ°ĒåÖŠ¼ÓČėµØ·ÆæÉŅŌŹ¹µ°°×ÖŹ·¢ÉśŃĪĪö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
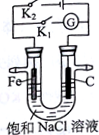 ČēĶ¼ĖłŹ¾£¬½«Ģś°ōŗĶŹÆÄ«°ō²åČėŹ¢ÓŠ±„ŗĶNaClČÜŅŗµÄUŠĶ¹ÜÖŠ£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø””””£©
ČēĶ¼ĖłŹ¾£¬½«Ģś°ōŗĶŹÆÄ«°ō²åČėŹ¢ÓŠ±„ŗĶNaClČÜŅŗµÄUŠĶ¹ÜÖŠ£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø””””£©| A£® | K1±ÕŗĻ£¬ĻņĢś°ōø½½üµĪČėK3[Fe£ØCN£©6]ČÜŅŗ£¬ÓŠĄ¶É«³Įµķ³öĻÖ | |
| B£® | K1±ÕŗĻ£¬µēĮ÷·½ĻņÓÉĢś°ō¾µ¼ĻßĮ÷ĻņŹÆÄ«°ō | |
| C£® | K2±ÕŗĻ£¬Ģ¼°ōŹĒŅõ¼« | |
| D£® | K2±ÕŗĻ£¬µēĀ·ÖŠĶعż0.2NAøöµē×ÓŹ±£¬Į½¼«¹²²śÉś4.48LĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2O”śNaOH | B£® | NaHCO3”śNa2CO3 | C£® | SiO2”śH2SiO3 | D£® | NH3”śNO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
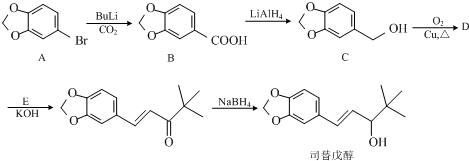
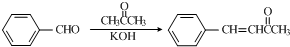
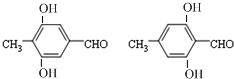 £ØČĪŅāŅ»ÖÖ£©£»£®
£ØČĪŅāŅ»ÖÖ£©£»£®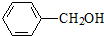 ĪŖŌĮĻÖʱø
ĪŖŌĮĻÖʱø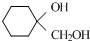 µÄ·“Ó¦ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£©£®
µÄ·“Ó¦ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4+Cl2$\stackrel{¹āÕÕ}{”ś}$CH3Cl+HC1 | B£® | 2CH3CH2OH+02$\stackrel{Cu”¢”÷}{”ś}$2CH3CH0+2H20 | ||
| C£® | 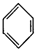 +HNO3$”ś_{50-60”ę}^{ÅØĮņĖį}$ +HNO3$”ś_{50-60”ę}^{ÅØĮņĖį}$ +H2O +H2O | D£® | nCH2=CH2$\stackrel{Ņ»¶ØĢõ¼ž}{”ś}$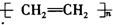 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com