
| A. | SO2和湿润的Cl2都有漂白性,推出二者混合后漂白性更强 | |
| B. | 根据溶液的pH与溶液酸碱性的关系,推出pH=7.0的溶液一定显中性 | |
| C. | 根据F、Cl、Br、I非金属性依次减弱,推出HF、HC1、HBr、HI的还原性依次增强 | |
| D. | 结构和组成相似的物质,沸点随相对分子质量增大而升高,因此NH3沸点低于PH3 |
分析 A、二氧化硫和氯气在水溶液中会发生氧化还原反应;
B、温度不定,pH=7时不一定为中性;
C、同一主族元素,元素的非金属性随着原子序数的增大而减小,非金属性越强的元素,其氢化物还原性越弱;
D、氨气中含氢键.
解答 解:A、等物质的量的二氧化硫和氯气在水溶液中会发生氧化还原反应生成盐酸和硫酸,不再具有漂白性,故A错误;
B、温度不定,pH=7时不一定为中性,如温度在100℃时,pH=6时溶液呈中性,故B错误;
C、非金属的非金属性越强,还原性越弱,F、C1、Br、I的非金属性逐渐减弱,所以其还原性依次增强,故C正确;
D、氨气中含氢键,沸点高于PH3,对不含氢键的,且结构和组成相似的物质,沸点随相对分子质量增大而升高,故D错误;
故选C.
点评 本题考查了物质的性质方面的知识,难度适中,解题时要注意一般规律与特殊情况的关系,以及规律所适用的条件等.


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:选择题
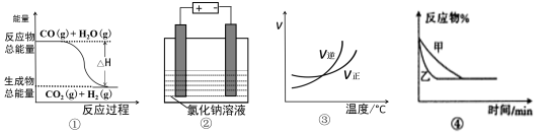
| A. | 图①表示可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0 | |
| B. | 图②表示用惰性电极电解足量氯化钠溶液.一段时间后,两极上可收集到相等体积的气体 | |
| C. | 图③表示可逆反应:A2(g)+3B2(g)?2AB3(g)△H<0 | |
| D. | 图④表示压强对可逆反应2A(g)+B(g)?3C(g)+D(s)的影响,乙压强大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 西维因分子式为C12H10NO2 | |
| B. | 西维因苯环上一溴取代产物有4种情况 | |
| C. | 可用FeCl3溶液检验西维因是否发生水解 | |
| D. | 在Ni催化下lmol西维因最多能与6molH2加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
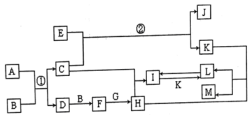
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
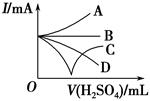 向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氢氧化钠溶液鉴别MgCl2溶液、AlCl3溶液 | |
| B. | 利用丁达尔效应鉴别Fe(OH)3胶体与FeCl3溶液 | |
| C. | 用干燥的红色石蕊试纸鉴别NH3和HCl气体 | |
| D. | 用氯化钙溶液鉴别Na2CO3溶液和NaHCO3两种溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热的纯碱溶液去油污效果比冷的纯碱溶液去油污效果好 | |
| B. | 加热稀醋酸溶液其pH 稍有减小 | |
| C. | 实验室制FeCl3溶液时,把FeCl3固体溶于浓盐酸中,再加水稀释到所需的浓度 | |
| D. | 草木灰与铵态氮肥不能混合使用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com