
【题目】某试液中只可能含有下列K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2-中的若干种离子,离子浓度均为0.1mol·L-1。某同学进行了如下实验:
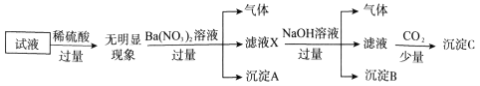
下列说法正确的是( )
A. 无法确定原试液中是否含有Al3+、Cl-
B. 滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C. 无法确定沉淀C的成分
D. 原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42-
【答案】D
【解析】
根据实验现象分析,加入过量稀硫酸无明显变化,说明无CO32-,无AlO2-;加入硝酸钡有气体,说明有亚铁离子存在且被氧化,沉淀为硫酸钡;加入NaOH有气体,说明存在铵根离子,气体为氨气,沉淀B为红褐色氢氧化铁沉淀;通入少量CO2产生沉淀,溶液呈碱性且含有钡离子,所以沉淀C为碳酸钡,不能说明存在Al3+;因为存在的离子浓度均为0.1mol·L-1,从电荷的角度出发,只能含有NH4+、Fe2+、Cl-、SO42-,才能保证电荷守恒;
A. 通过上述分析,原试液没有Al3+,有Cl-,故A错误;
B. 根据上述分析,滤液X中大量存在的阳离子有NH4+、Ba2+和Fe3+,故B错误;
C. 沉淀C的成分为碳酸钡,故C错误;
D. 根据上述分析原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42-,故D正确,
故选D。


科目:高中化学 来源: 题型:
【题目】卤代烃在碱性醇溶液中能发生消去反应。例如,

该反应式也可表示为

下面是几种有机化合物的转化关系:

(1)根据系统命名法,化合物A的名称是_____________。
(2)上述框图中,①_________是反应,③___________是反应。
(3)化合物E是重要的工业原料,写出由D生成E的化学方程式:_________。
(4)C2的结构简式是,F1的结构简式是______________,F1与F2互为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①CH3CH=CHCH3、② ![]() 、③
、③![]() 、④CH3CH2CH(C2H5)2、⑤35Cl、⑥O2、⑦-CH3、⑧CH2=CH-CH=CH2、⑨37Cl、⑩O3
、④CH3CH2CH(C2H5)2、⑤35Cl、⑥O2、⑦-CH3、⑧CH2=CH-CH=CH2、⑨37Cl、⑩O3
(1)互为同系物的有___________________(用序号表示)。
(2)互为同位素的有___________________(用序号表示)。
(3)③的系统名称_____________________,②的系统名称_____________________。
(4)写出⑧与Br2 按照1:1发生加成反应所得产物的结构简式______________________________。
(5)等物质的量的⑦和⑩的电子数之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理在生产生活中有广泛的应用。下列叙述正确的是
A.开发新技术可将水分解成氢气、氧气并释放能量
B.研制新型催化剂可提高汽车尾气的平衡转化率
C.燃料电池能将化学能完全转化为电能
D.为防止金属管道被腐蚀,应将金属管道与电源负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的描述中,正确的是
A.乙醇在Cu催化下能被氧气氧化成乙醛
B.乙烯使高锰酸钾溶液和溴水褪色的原理相同
C.油脂可以水解生成氨基酸
D.葡萄糖能发生银镜反应和水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中可以作为2NO2(g) ![]() 2NO(g)+O2(g)达到平衡状态的标志是( )
2NO(g)+O2(g)达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2;②单位时间内生成n mol O2的同时生成2n mol NO;③混合气体的颜色不再改变;④混合气体的密度不再改变的状态;⑤混合气体的平均相对分子质量不再改变的状态;⑥混合气体中NO与O2的物质的量之比保持恒定;⑦混合气体中NO与NO2的物质的量之比保持恒定
A. ①③⑤⑦ B. ②④⑤ C. ①③④ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)“高分一号”卫星使用了大功率运载火箭,火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),其反应为N2H4(l)+2H2O2(l)=N2(g)+4H2O(g),该反应生成1molH2O(g)释放出160.4kJ热量。
①H2O2的电子式为______。
②若反应后,O-H键增加了16mol,则反应释放出的热量为______kJ。
(2)镍氢蓄电池具有能量密度大、电压高、可多次反复充放电等特性,该电池放电时,正极反应式为2NiOOH+2H2O+2e-=2Ni(OH)2+2OH-,负极反应式为H2+2OH-+2e-=2H2O。
①该镍氢蓄电池放电时的电池总反应为____。
②该电池放电时,OH-向____(填“正极”或“负极”)移动。
③假设该电池放电时有2.408×1024个电子从负极流向正极,则消耗的H2在标准状况下的体积为____L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气(如图),下列对于试管内发生的反应及现象的说法正确的是
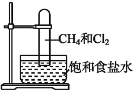
A. 此反应无光照也可发生
B. 甲烷和Cl2反应后的产物只有CH3Cl和HCl
C. 盛放饱和食盐水的水槽底部会有少量晶体析出
D. CH4和Cl2完全反应后液面上升,液体充满试管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )

A. a通入CO2,然后b通入NH3,c中放碱石灰
B. b通入NH3,然后a通入CO2,c中放碱石灰
C. a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D. b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com