
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个
“封管实验”(夹持装置未画出),判断下列说法正确的是( )

A.加热时,①上部汇集了固体NH4Cl,说明NH4Cl的热稳定性比较好
B.加热时,②、③溶液均变红,冷却后又都变为无色
C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内
气体颜色变浅
D.四个“封管实验”中所发生的化学反应都是可逆反应
科目:高中化学 来源: 题型:
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
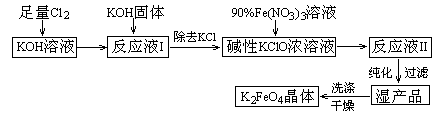 |

已知:① 2KOH + Cl2 → KCl + KClO + H2O(条件:温度较低)
② 6KOH + 3Cl2 →5KCl + KClO3 + 3H2O(条件:温度较高)
③ 2Fe(NO3)3 +3KClO+10KOH →2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
(1)该生产工艺应在温度 (填“较高”或“较低”)的情况下进行;
(2)写出工业上制取Cl2的化学方程式 ;
(3)K2FeO4具有强氧化性的原因 ;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度约为 。
(5)在“反应液I”中加KOH固体的目的是 (选填序号)。
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为 KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品 (写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ca2+
B.用玻璃棒蘸取新制氯水,点在PH试纸的中央,与标准比色卡比较,测定氯水的PH
C.某溶液与NaOH溶液共热,产生使湿润红色石蕊试纸变蓝气体,说明原溶液中存在NH4+
D.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化钠能与水发生反应:2Na2O2+2H2O=4NaOH+O2↑,某同学用该反应制取标准状况下的1.12L氧气。
(1)计算至少需要称取过氧化钠的质量。
(2)若反应得到氢氧化钠溶液的体积是200mL,计算该溶液中溶质的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
用3g铁粉与30ml,3mol/L的盐酸反应制取氢气,若要加快产生氢气的速率
可采取措施是( )
A.改用浓H2SO4 B.改用6mol/L的盐酸
C.改用6mol/L的HNO3 D.改用6g的铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备H2的一种重要方法是:
 CO(g) + H2O(g)
CO(g) + H2O(g)  CO2 (g) + H2(g) △H=Q kJ/mol
CO2 (g) + H2(g) △H=Q kJ/mol
已知
该反应的平衡常数K与温度T的关系右上图所示。若在一固定的密闭容器中,
850℃ 时发生上述反应,测得容器内各物质的浓度 (mol/L)随时间的变化
关系如下表:

已知:850℃ 时该反应的化学平衡常数K = 1.0 ,请回答下列问题:
(1) Q 0(填“ > ”、“ = ”或“<” )。
若在850℃时向反应容器中充人H2O(g),K 值 (填增大、减小、不变)
(3)上表中 c2为 mol/L , CO(g)的转化率为 (保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是:
A、向500mL 1 mol /LNa2CO3溶液中,滴加600mL 1 mol /LHCl 得到标况下
CO2体积为2.24L
B、电解精炼铜时,若阴极得到2摩尔电子,则阳极质量减少64克
C、将208 g BaCl2固体溶解在1 L水中,形成的溶液的浓度为1 mol·L-1
D、可用pH试纸测得氯水的酸性强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com