
【题目】已知常温下浓度为0.1mol/L的几种溶液的pH如下表。下列有关说法不正确的是
溶质 | NaF | Na2CO3 | NaClO | NaHCO3 |
pH | 7.5 | 11.6 | 9.7 | 8.3 |
A. 同温度同浓度下,酸性由强到弱的顺序为:HF>H2CO3>HClO
B. 水解方程式:F-+H2O![]() HF+OH-的平衡常数约为9×10-13
HF+OH-的平衡常数约为9×10-13
C. 将CO2通入0.lmol/LNa2CO3溶液至溶液呈中性,则溶液中:c(CO32-)+c(HCO3-)+ c(H2CO3)=0.2mol/L
D. 等物质的量的NaF和HF混合溶液中粒子浓度大小关系为:c(F-)>c(Na+)> >c (H+)>c(OH-)
【答案】C
【解析】
A.由表格数据可知,0.1mol/L的弱酸盐溶液中水解程度由大到小的顺序为Na2CO3>NaClO>NaHCO3>NaF,根据盐类水解规律“越弱越水解”,可推知对应酸的酸性由强到弱的顺序为:HF>H2CO3>HClO>HCO3-,A项正确;
B.由表格数据知0.1mol/LNaF溶液中pH=7.5,常温下该溶液中c(OH-)=![]() =
=![]() =10-6.5mol/L,c(HF)= 10-6.5mol/L-10-7.5mol/L=9×10-7.5mol/L,根据F-+H2O
=10-6.5mol/L,c(HF)= 10-6.5mol/L-10-7.5mol/L=9×10-7.5mol/L,根据F-+H2O![]() HF+OH-得水解平衡常数Kh=
HF+OH-得水解平衡常数Kh=![]() =
=![]() ≈9×10-13,B项正确;
≈9×10-13,B项正确;
C. 因Na2CO3溶液和NaHCO3溶液均呈碱性,只有H2CO3溶液呈酸性,所以将CO2通入0.lmol/LNa2CO3溶液至溶液呈中性时,发生的反应有Na2CO3+CO2+H2O=2NaHCO3,CO2+H2O=H2CO3,所得溶液为NaHCO3(浓度为0.2mol/L)和H2CO3的混合溶液,根据物料守恒,溶液中有c(CO32-)+c(HCO3-)+ c(H2CO3)>0.2mol/L,C项错误;
D.由B项分析知,相同温度下HF的电离常数Ka=![]() ≈
≈![]() =0.011,故有Ka>Kh,说明HF的电离程度大于NaF的水解程度,所以等物质的量的NaF和HF混合溶液中粒子浓度大小关系为:c(F-)>c(Na+)> c (H+)>c(OH-),D项正确;答案选C。
=0.011,故有Ka>Kh,说明HF的电离程度大于NaF的水解程度,所以等物质的量的NaF和HF混合溶液中粒子浓度大小关系为:c(F-)>c(Na+)> c (H+)>c(OH-),D项正确;答案选C。


科目:高中化学 来源: 题型:
【题目】实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体,经历了下列过程(已知 Fe3+在 ph=5时沉淀完全).其中分析错误的是
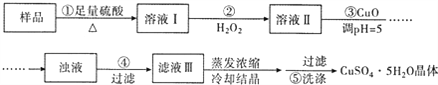
A. 步骤②发生的主要反应为:2Fe2++H2O2+2H+=2Fe3++2H2O
B. 步骤②可用氯水、硝酸等强氧化剂代替H2O2
C. 步骤③用 CuCO3代替CuO也可调节溶液的pH
D. 步骤⑤ 的操作为:向漏斗中加入少量冷的蒸馏水至浸没晶体,待水自然流下,重复操作 2~3次
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)选择适宜的材料和试剂设计一个原电池,完成下列反应:Zn+CuSO4=ZnSO4+Cu。
①画出装置图:___。
②电极材料和电解质溶液各是什么___。?
③写出电极反应式:负极:___;正极:___。
(2)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25克,铜表面析出了氢气___L(标准状况下)。导线中通过___mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
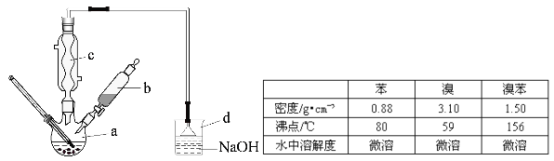
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了 气体。继续滴加至液溴滴完,装置d的作用是 ;
(2)液溴滴完后,经过下列步骤分析提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是 ③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤,加入氯化钙的是 ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯,下列操作中必须的是 (填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是 (填入正确选项前的字母)。
A.25mL B. 50mL C.250mL D.500mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 向溴化亚铁溶液中通入少量氯气:2Fe2++Cl2===2Fe3++2Cl-
B. 苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O―→2C6H5OH+CO![]()
C. 向硫酸氢钠溶液中滴入氢氧化钡溶液至中性:H++SO![]() +Ba2++OH-===BaSO4↓+H2O
+Ba2++OH-===BaSO4↓+H2O
D. 将氢氧化铁粉末加入氢碘酸中:Fe(OH)3+3H+===Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学—有机化学基础)瘦肉精又名克伦特罗(4-氨基-α-叔丁胺甲基-3,5-二氯苯甲醇),是一种β2肾上腺素受体激动剂,临床上用于治疗哮喘。可由下图所示路线合成:

其中X表示某中间物质,请回答下列问题。
(1)判断反应④的反应类型 。
(2)书写反应③所代表的化学反应方程式:
。
(3)试推断中间物质X的结构简式: 。
(4)对氨基苯乙酮![]() 的同分异构体有多种,请写出符合以下条件的其中任意一种
的同分异构体有多种,请写出符合以下条件的其中任意一种
a.苯环与氨基相连 b.与新制的Cu(OH)2悬浊液加热,有红色物质生成
c.苯环上有2个取代基
(5)①②③代表的整个反应过程完成了苯胺对位的酰基化,也完成了对 (填官能团名称)的保护,同时也避免了一些副反应的发生。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的短周期主族元素。X分别与Y、Z、W结合形成质子数相同的甲、乙、丙三种分子。丁为无色气体,遇空气变红棕色;丙的水溶液可刻蚀玻璃。
上述物质有如图转化关系:

下列说法错误的是
A. 四种元素形成的单质中W的氧化性最强
B. 甲、乙、丙中沸点最高的是丙
C. 甲常用作致冷剂
D. 甲、乙分子均只含极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸D(β-苯基丙烯酸)用于制备化妆品、香皂的香精,乜可制造局部麻醉剂、杀菌剂、止血药、植物生长促进剂、防腐剂、感光树脂等。下列是肉桂酸D的合成与应用的反应路线:
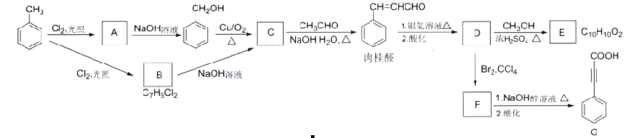
已知:![]()
(1)A的分子式是_______,A生成苯甲醇的反应类型是________。
(2)C的结构简式是_______,肉柱醛中的官能团名称是________。
(3)E是一种合成香精的定香剂,已知E为反式结构,则其结构简式为_______。
(4)在G中共直线的原子共有_______个,1molB转化为C最多消耗_______mol NaOH
(5)写出上图中F与NaOH醇溶液共热时的化学方程式________。
(6)P是E的同分异构体,写出符合下列条件的P的键线式_______。
①有两个相同的官能团;②能与新制氢氧化铜悬浊液作用产生砖红色沉淀;③含有苯环,核磁共振氢谱有三组面积之比为2︰2︰1的峰。
(7)以乙醇为原料,设计制备高分子化合物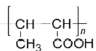 的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件,无机试剂任选)______
的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件,无机试剂任选)______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回收的废旧锌锰干电池经过处理后可得到锰粉(含MnO2、Mn(OH)2、Fe和炭粉等),由锰粉为主要原料制备高性能磁性材料碳酸锰(MnCO3)的工艺流程如下:
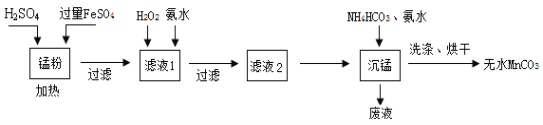
已知:①2H2SO4 + MnO2 + 2FeSO4 = MnSO4 + Fe2(SO4)3 + 2H2O
②部分氢氧化物的Ksp(近似值)如下表(25 ℃)
物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp | 10-13 | 10-17 | 10-38 |
根据上图流程及有关数据回答下列问题。
(1)锰粉酸溶时,过量FeSO4所起的作用为______________________。
(2)往滤液1中先加入H2O2的目的是氧化Fe2+,该反应的离子方程式为________________,后加入氨水的目的是调节pH除去杂质离子,使滤液中的杂质离子沉淀完全(残留在溶液中的离子浓度≤ l0-5 mol·L-1),常温下测得溶液中c(Mn2+)=0.1 mol·L-1,则需调节溶液的pH范围为_______________。
(3)沉锰工序中,加入氨水的目的是(从化学平衡移动的角度解释)___________,沉锰工序中判断沉淀已经洗涤干净的实验操作是________________________________。
(4)沉锰后废液中的主要成份为_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com