
下列说法正确的是( )
A.甲烷、乙烯和苯在工业上都可通过石油分馏得到
B.苯油脂均不能使酸性KMnO4溶液褪色
C.乙烯和苯都能使溴水褪色,褪色原理相同
D.甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同
科目:高中化学 来源:2015-2016学年河南省周口市高一下学期期中考试化学试卷(解析版) 题型:选择题
100 mL 6 mol·L-1的H2SO4溶液跟过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的
①Na2CO3溶液 ②水 ③K2SO4溶液 ④KNO3溶液
A.①③ B.②③ C.①④ D.②④
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:实验题
废弃物的综合利用既有利于节约资源,又有利于保护环境。工业上利用铅浮渣(主要成分是PbO、Pb还含有少量的Ag、CaO)可制备硫酸铅。制备流程图如下:

下表是25℃ 时某些盐的浓度积常数:
化学式 | CaSO4 | Ag2SO4 | PbSO4 |
Ksp | 4.9×10-5 | 1.2×10-5 | 1.6×10-8 |
(1)实验室用75%的硝酸来配制15%的硝酸溶液,不需用到的玻璃仪器有 (填标号)。
A.烧杯 B.量筒 C.容量瓶 D.锥形瓶 E.玻璃棒
(2)步骤I有NO产生,浸出液中含量最多的金属阳离子为 Pb2+,写出Pb参加反应的化学方程式 ,为防止Ag被溶解进入溶液,步骤I操作时应注意 。
(3)母液可循环利用于步骤I,其溶质主要是 (填一种物质化学式),若母液中残留的 SO42-过多,循环利用时可能出现的问题是 。
(4)粗PbSO4 产品含有的杂质是____________,需用 溶液多次洗涤,以得到纯净的PbSO4。
(5)铅蓄电池放电时正极的电极反应式为 。如果用铅蓄电池做电源电解饱和食盐水制取Cl2,已知某铅蓄电池中硫酸溶液的体积为0.80 L,电解前硫酸溶液浓度为4.50 mol·L-1,当制得4.48 LCl2时(在标准状况下),求理论上电解后电池中硫酸溶液的浓度为(假设电解前后硫酸溶液的体积不变)_________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二下期中化学试卷(解析版) 题型:选择题
某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol醇和2mol乙酸,该醇的分子式为( )
A.C14H18O5
B.C14H16O4
C.C14H22O3
D.C14H10O3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二下期中化学试卷(解析版) 题型:选择题
有下列有机反应类型:①消去反应②水解反应③加聚反应④加成反应⑤还原反应⑥氧化反应,以丙醛为原料制取1,2一丙二醇,所需进行的反应类型依次是( )
A.⑤①④② B.⑥④②① C.①③②⑤ D.⑤②④①
查看答案和解析>>
科目:高中化学 来源:2016届湖南省等四校高三联考化学试卷(解析版) 题型:填空题
研究硫元素及其化合物的性质具有重要意义
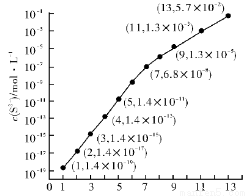
(1)25 ℃,在0.10 mol • L-1HA溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如右图(忽略溶液体积的变化、H2S的挥发)。
①pH=11 时,溶液中的 c(H2S)+c(HS-)= mol•L-1。(保留3位有效数字)
②某溶液含0.010 mol • L-1 Fe2+、未知浓度的Mn2+和0.10 mol•L-1H2S,当溶液pH= 时,Fe2+开始沉淀;当Mn2+开始沉淀时,溶液中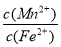 = 。
= 。
[已知:Ksp(FeS)=1.4×10-19,Ksp(MnS)=2.8×10-13]
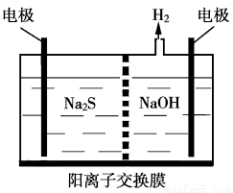
(2)硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。其中一种是将烧碱吸收H2S后的溶液加入到如图所示的电解池 的阳极区进行电解。请写出阳极的电极反应式 ,同时阳极区还发生(n—1)S+S2-=Sn2-。电解后阳极区的溶液用稀硫酸酸化,产生淡黄色浑浊,其离子方程式为 。
(3)25℃,两种酸的电离平衡常数如下表。
Ka | Ka2 | |
H2SO3 | 1.3X10-2 | 6.3X10-8 |
H2CO3 | 4.2X10-7 | 5.6X10-11 |
实验室常用饱和NaHCO3溶液除去CO2中少量的SO2,请写出SO2和NaHCO3溶液反应的主要离子方程式 。[
查看答案和解析>>
科目:高中化学 来源:2016届湖南省等四校高三联考化学试卷(解析版) 题型:选择题
2015年10月,屠哟哟获得诺贝尔生理学或医学奖,理由是她发现了青蒿素,这种药品可以有效降低疟疾患者的死亡率。她成为首获科学类诺贝尔奖的中国人。青蒿素两步可合成得到治疗疟疾的药物青蒿琥酯。下列有关说法正确的是
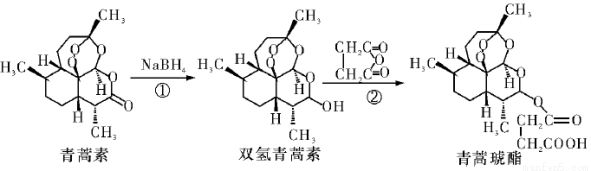
A.青蒿素分子式为C15H24O5
B.反应②原子利用率为100%
C.该过程中青蒿素生成双氢青蒿素属于氧化反应
D.1 mol青蒿琥酯与氢氧化钠溶液反应,最多消耗1 mol氢氧化钠
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.放热反应不一定不需要加热,但吸热反应一定需要加热
B. 中和反应都是放热反应
C.氢气燃烧放出大量的热,说明参加反应的氢气和氧气总能量比生成物水的总能量低
D.C与CO2反应是吸热反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期中化学试卷(解析版) 题型:选择题
现有部分短周期元素的性质或原子结构如下表:
元素符号 | 元素性质或原子结构 |
T | M层上的电子数是原子核外电子层数的2倍 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
下列叙述中不正确的是
A.14X可用与测定文物年代 B.Z的非金属性比T强
C.Y和T位于同一主族 D.X元素形成的化合物种类很多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com