



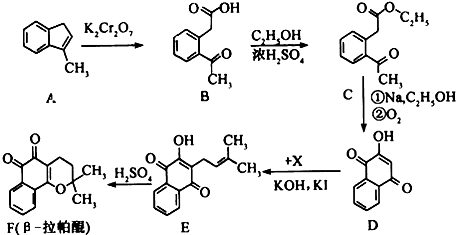
 ,结合各物质转化关系,A为苯环上连有-C4H9基团,且与苯环相连的碳上至少有一个氢原子,这样的结构烃基为-CH2CH2CH2CH3、-CH2CH(CH3)2、-CH(CH3)CH2CH3共三种,A发和信息中的反应在-C4H9的对位引入醛基,B与氢气加成将醛基还原成羟基,C发生酯化反应生成D,D发生氧化反应得E,E在酸性条件下水解得F,据此答题;
,结合各物质转化关系,A为苯环上连有-C4H9基团,且与苯环相连的碳上至少有一个氢原子,这样的结构烃基为-CH2CH2CH2CH3、-CH2CH(CH3)2、-CH(CH3)CH2CH3共三种,A发和信息中的反应在-C4H9的对位引入醛基,B与氢气加成将醛基还原成羟基,C发生酯化反应生成D,D发生氧化反应得E,E在酸性条件下水解得F,据此答题; ,
, ;
; ,结合各物质转化关系,A为苯环上连有-C4H9基团,且与苯环相连的碳上至少有一个氢原子,这样的结构烃基为-CH2CH2CH2CH3、-CH2CH(CH3)2、-CH(CH3)CH2CH3共三种,A发和信息中的反应在-C4H9的对位引入醛基,B与氢气加成将醛基还原成羟基,C发生酯化反应生成D,D发生氧化反应得E,E在酸性条件下水解得F,
,结合各物质转化关系,A为苯环上连有-C4H9基团,且与苯环相连的碳上至少有一个氢原子,这样的结构烃基为-CH2CH2CH2CH3、-CH2CH(CH3)2、-CH(CH3)CH2CH3共三种,A发和信息中的反应在-C4H9的对位引入醛基,B与氢气加成将醛基还原成羟基,C发生酯化反应生成D,D发生氧化反应得E,E在酸性条件下水解得F, ,
, ;
;


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

 .
. :
:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向1 mo1?L-l CH3COOH溶液中加入少量CH3COONa固体,由于CH3COONa水解显碱性,所以溶液的pH升高 | ||||||||||
B、25℃时,将a mo1?L-l氨水与0.01 moI?L-1盐酸等体积混合,反应完全时溶液中Kb=
| ||||||||||
C、根据下表数据可以计算出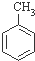 (g)+3H2(g)→ (g)+3H2(g)→ (g)的焓变 (g)的焓变
| ||||||||||
| D、已知298K时,MgCO3的Ksp=6.82×10-6,溶液中c(Mg2+)=0.0001 mol?L-1,c(CO32-)=0.0001 mol?L-1,此时Mg2+和CO32-不能共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D |
| 制备并收集氨气 | 比较Na2CO3与NaHCO3的稳定性 | 用NaOH溶液滴定锥形瓶中的盐酸溶液 | 制备乙酸乙酯 |
 |  |  |  |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向鸡蛋白溶液中滴入HgCl2溶液 | 有白色沉淀 | 蛋白质发生盐析 |
| B | 向溶液X中滴加BaCl2溶液 | 有白色沉淀 | X中一定含有SO42- |
| C | AgCl饱和溶液中加入少量NaI溶液 | 产生黄色沉淀 | Ksp(AgI)>Ksp(AgCl) |
| D | 向加入了几滴酚酞试液的Na2CO3溶液中滴加BaCl2溶液 | 红色逐渐退去 | Na2CO3溶液中存在水解平衡 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com