
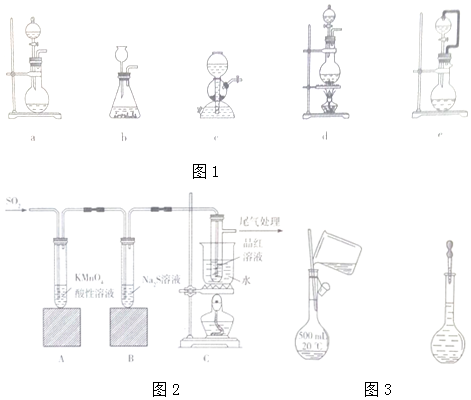
���� ��1���ٸ��ݷ�Ӧ���״̬�ͷ�Ӧ����ѡ��װ�ã�
��Ϊ���ڶ��������������Ӧѡ��Ũ���ᣬ��Ũ�ȹ��ߣ����Ტδ��ȫ���룬���Է�����ʽ���ڣ���Na2SO3��H2SO4�ķ�Ӧ����H2SO4��������ӵ�״̬�²���˳�����еģ���ͨ������80%��ŨH2SO4��
��2�����������л�ԭ�ԡ������Ժ�Ư���ԣ�ͨ��ʢ�����Ը�����ص�Aװ�ã������������Ը��������ɫ��ͨ��ʢ��������Һ��Bװ�ã�������̬���з�Ӧ���ɵ���ɫ��S���ʣ�ͨ��ʢ��Ʒ����Һ��Cװ�ã�ʹƷ����Һ��ɫ�����ȣ���ɫ�ָ����ݴ˷�����
��3����NaOH��SO2��Ӧ�����������ƣ�
������250mL��Һѡ��250mL����ƿ����ͷ�ιܲ�����������ƿ�ڣ�������Ⱦ��Һ��
��� �⣺��1����Na2SO3�����ᷴӦ��ȡSO2��Ϊ��Һ�������ͣ�ae���ɣ���ѹ©����Ӧ��ƽ�����У�����˳�����ٵ��£�
�ʴ�Ϊ��ae��e��
��Ϊ���ڶ��������������Ӧѡ��Ũ���ᣬ��Ũ�ȹ��ߣ����Ტδ��ȫ���룬���Է�����ʽ���ڣ���Na2SO3��H2SO4�ķ�Ӧ����H2SO4��������ӵ�״̬�²���˳�����еģ���ͨ������80%��ŨH2SO4��
�ʴ�Ϊ��C��
��2���ٶ��������л�ԭ�ԣ�ʹ���Ը��������ɫ��
�ʴ�Ϊ�����Ը��������Һ��ɫ��
�ڶ���������Ư���ԣ�ʹƷ����Һ��ɫ����SO2��Ʒ�����ɲ��ȶ������ʣ����ȣ�Ʒ����ɫ�ָ�������������������ǣ���ȼ�ƾ��ƣ����ȣ��Թ���Ʒ����Һ�ָ�Ϊ��ɫ��
�ʴ�Ϊ����ȼ�ƾ��ƣ����ȣ��Թ���Ʒ����Һ�ָ�Ϊ��ɫ��
����֤SO2�����Ե�װ����B�������������������̬���з�Ӧ���ɵ���ɫ��S���ʣ���ѧ����ʽΪ��SO2+2Na2S+2H2O=4NaOH+3S����
�ʴ�Ϊ��B��SO2+2Na2S+2H2O=4NaOH+3S����
��3����NaOH��Һ����SO2β�������ӷ���ʽ�ǣ�2OH-+SO2=SO32-+H2O��
�ʴ�Ϊ��2OH-+SO2=SO32-+H2O��
������250mL��Һѡ��250mL����ƿ����ͷ�ιܲ�����������ƿ�ڣ�������Ⱦ��Һ��
�ʴ�Ϊ������ѡ��500mL����ƿ������ʱ����ͷ�ιܲ�����������ƿ�ڣ�
���� ���⿼���˶���������Ʊ����漰ʵ��װ�õ�ѡ�����ʵ����ʡ����ӷ���ʽ����д��֪ʶ�㣬��Ŀ�Ѷ��еȣ��������ʵ����ʲ���������ǹؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

| ��� | ʵ��Ŀ�� | ̼��/g | ����/g | ����/% |
| �� | Ϊ����ʵ�������� | 0.5 | 2.5 | 90.0 |
| �� | �� | 0.5 | 2.5 | 36.0 |
| �� | ̼��������Ӱ�� | 0.2 | �� | 90.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢۢݢߢ� | B�� | �٢ܢޢ� | C�� | �٢ڢۢߢ� | D�� | �ڢۢݢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2CO3+H2SO4�TCO2��+H2O+Na2SO4 | B�� | CO2+2NaOH�TNa2CO3+H2O | ||
| C�� | CO2+2Mg$\frac{\underline{\;��ȼ\;}}{\;}$ 2MgO+C | D�� | CO2+Na2O=Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ������һ����ͭ | |
| B�� | ������һ������ | |
| C�� | ��������һ����ͭ������һ������ | |
| D�� | ��Һ��һ������FeSO4��һ��û��CuSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��С | B�� | ��� | C�� | ���� | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijͬѧͨ��ʵ���о��Ƽ��仯������й����ʣ���ش�������⣮
ijͬѧͨ��ʵ���о��Ƽ��仯������й����ʣ���ش�������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C+O2$\stackrel{��ȼ}{��}$CO2 | B�� | C��s��+O2��g��$\stackrel{��ȼ}{��}$CO2��g��+393.5kJ | ||
| C�� | C��s��+O2��g��$\stackrel{��ȼ}{��}$CO2��g�� | D�� | C��s��+O2��g��=CO2��g��+393.5kJ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com