
| A. | 原子序数B>A>C | B. | 原子半径A>B>C | ||
| C. | 离子半径A2->B2+>C- | D. | 原子最外层电子数C>A>B |
分析 A、B、C为三种短周期元素,结合离子所带电荷可知,A是第ⅥA族,B是第ⅡA族,C位于第ⅦA,B2+与C-具有相同的电子层结构,则B位于C的下一周期,由于A、B同周期,则A、B处于第三周期,C处于第二周期,则A为S、B为Mg、C为F,周期自左向右,原子半径逐渐减小,同主族自上而下原子半径逐渐增大,而电子层结构相同核电荷数越大离子半径越小,以此解答该题.
解答 解:A、B、C为三中短周期元素,结合离子所带电荷可知,A是第ⅥA族,B是第ⅡA族,C位于第ⅦA,B2+与C-具有相同的电子层结构,则B位于C的下一周期,由于A.B同周期,则A、B处于第三周期,C处于第二周期,则A为S、B为Mg、C为F,
A.A为S、B为Mg、C为F,原子序数:S>Mg>F,故A错误;
B.同周期自左向右,原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则原子半径是:Mg>S>F,故B错误;
C.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径:S2->F->Mg2+,故C错误;
D.A为S、B为Mg、C为F,原子核外最外层电子数:F>S>Mg,故D正确,
故选D.
点评 本题以周期表中元素的推断为载体,考查学生对元素周期表的熟悉程度、微粒半径比较等,是高考中的常见题型,注意把握原子的结构和元素周期率、周期表知识,题目难度中等.


 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:解答题
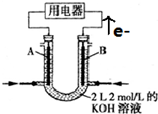
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
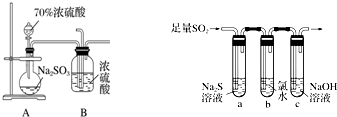
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度 | B. | 加入氯化钠溶液 | C. | 加入Na2CO3溶液 | D. | 加入浓盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度相同、体积相同的O2和N2 | B. | 压强相同、体积相同的H2和O2 | ||
| C. | 质量相等、密度不等的N2和CO | D. | 体积相等、密度相等的CO和C2H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中水电离出的c(H+)=10-3mol/L | |
| B. | 溶液中c(A-)=10-3mol/L | |
| C. | 溶液中加水稀释,促进HA电离,溶液的c(H+)增大,但k不变 | |
| D. | 与0.1mol/LNaOH溶液等体积混合后所得溶液中(体积变化忽略不计)c(Na+)═c(A-)+c(OH-)-c(H+)=0.1 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 16g氧气 | B. | 0.1mol甲烷分子(CH4) | ||
| C. | 1.8g水 | D. | 含3.01×1022个磷酸分子(H3PO4) |
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:选择题
常温下,将Cl2缓慢通入水中至饱和,然后再滴加0.1 mol·L-1的NaOH溶液,整个过程中溶液的pH变化曲线如图所示。下列选项正确的是
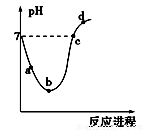
A.a点所示的溶液中[H+]=[Cl-]+[HClO]+[OH-]
B.b点所示的溶液中[H+]>[Cl-]>[HClO]>[ClO-]
C.c点所示的溶液中[Na+]=[HClO]+[ClO-]
D.d点所示的溶液中[Na+]>[ClO-]>[Cl-]>[HClO]
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com