
将SO2和O2以体积比为1:3混合后,通入接触室发生反应2SO2(g)+O2(g) ≒ 2 SO3(g), 达平衡时,在同温、同压下测得反应前与反应后混合气体的密度之比为71:80。求SO2的转化率?并回答SO2接触氧化为SO3时不采取加压措施的原因。
设反应前混合气体中SO2的体积为1 L,O2 应为3 L达平衡时SO2的转化的体积为x 。
2SO2(g)+O2(g) ≒ 2 SO3(g) 总体积
V/L(起始) 1 3 0 4L
V/L(转化) 2x x 2x
V/ L(平衡)1-2x 3-x 2x 4-x
根据气体的密度之比等于气体体积的反比,可得:
71:80=(4-x):4 x=0.45L,则转化的二氧化硫为0.9L,
二氧化硫的转化率为:0.9L÷1L×100%=90%
在工业上不加压,SO2的转化率就达90% 以上,已经很高,若再加压SO2的转化率提高不大,但对设备的要求要提高许多,故没有必要再加压。
这是一道关于化学平衡和转化率的综合计算题。根据相同条件下气体的密度之比等于同体积气体的质量之比,且反应前后质量守恒,可得出气体的密度之比等于气体体积的反比。 设反应前混合气体中SO2的体积为1 L,O2 应为3 L达平衡时SO2的转化的体积为x 。
2SO2(g)+O2(g) ≒ 2 SO3(g) 总体积
V/L(起始) 1 3 0 4L
V/L(转化) 2x x 2x
V/ L(平衡)1-2x 3-x 2x 4-x
根据气体的密度之比等于气体体积的反比,可得:
71:80=(4-x):4 x=0.45L,则转化的二氧化硫为0.9L,
二氧化硫的转化率为:0.9L÷1L×100%=90%
在工业上不加压,SO2的转化率就达90% 以上,已经很高,若再加压SO2的转化率提高不大,但对设备的要求要提高许多,故没有必要再加压。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
 利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.T℃时反应2SO2(g)+O2(g)AUTOTEXT<=>\*MERGEFORMAT 错误!未找到引用源.2SO3(g)过程中的能量变化如图所示,回答下列问题.
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.T℃时反应2SO2(g)+O2(g)AUTOTEXT<=>\*MERGEFORMAT 错误!未找到引用源.2SO3(g)过程中的能量变化如图所示,回答下列问题.
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
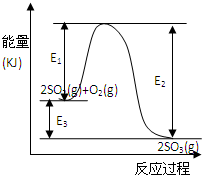 利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.T℃时反应2SO2(g)+O2(g)?2SO3(g)过程中的能量变化如图所示,回答下列问题.
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.T℃时反应2SO2(g)+O2(g)?2SO3(g)过程中的能量变化如图所示,回答下列问题.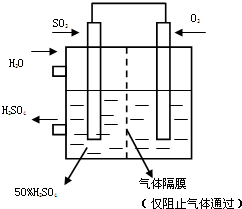
查看答案和解析>>
科目:高中化学 来源:2013-2014学年陕西省等五校高三第一次模拟考试理综化学试卷(解析版) 题型:填空题
运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义
(1)硫酸生产过程中2SO2(g)+O2(g) 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如右图所示,根据下图回答下列问题:
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如右图所示,根据下图回答下列问题:

①2SO2(g)+O2(g) 2SO3(g)的△H__________0(填“>”或“<”),
2SO3(g)的△H__________0(填“>”或“<”),
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中发生以上反应,能说明该反应已达到平衡的是???????? 。
A.体系的密度不发生变化???? ????????????? ? B.SO2与SO3的体积比保持不变
C.体系中硫元素的质量百分含量不再变化??? ?? D.单位时间内转移4 mol 电子,同时消耗2 mol SO3
E.容器内的气体分子总数不再变化
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g)  2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。

图1 ????? ? ? 图2?? ???? ? 图3
①该反应的平衡常数表达式为?????????? ,升高温度,平衡常数????????? (填“增大”或“减小”或“不变”)。
②由图2信息,计算0~10min内该反应的平均速率v(H2)=??????? ,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为??????? (填“a”或“b”或“c”或“d”)
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 ????? 点,温度T1 ?? T2(填“>”或“=”或“<”)
(3)若将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈???? 性,所得溶液中c(H+)- c(OH-)=??????????? (填写表达式)(已知:H2SO3:Ka1=1.7×10-2,Ka2=6.0×10-8,NH3·H2O:Kb=1.8×10-5)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年云南省部分名校高三第一次联考(11月)理综化学试卷(解析版) 题型:填空题
运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义
(1)硫酸生产过程中2SO2(g)+O2(g) 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图 所示,根据图回答下列问题:
所示,根据图回答下列问题:
①2SO2(g)+O2(g) 2SO3(g)的△H__________0(填“>”或“<”)。
2SO3(g)的△H__________0(填“>”或“<”)。
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中发生以上反应,能说明该反应已达到平衡的是 。
a.体系的密度不发生变化
b.SO2与SO3的体积比保持不变
c.体系中硫元素的质量百分含量不再变化
d.单位时间内转移4 mol 电子,同时消耗2 mol SO3
e.容器内的气体分子总数不再变化
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g) 2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。

图1 图2 图3
①该反应的平衡常数表达式为 ,升高温度,平衡常数 (填“增大”或“减小”或“不变”)。
②由图2信息,计算0~10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为 。
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1 T2(填“>”或“=”或“<”)
(3)若将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈 性,所得溶液中c(H+)- c(OH-)= (已知:H2SO3:Ka1=1.7×10-2,Ka2=6.0×10-8,NH3·H2O:Kb=1.8×10-5)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com