
 肼(N2H2)是火箭常用的高能燃料,常温下为液体,其球棍模型如图所示.肼能与双氧水发生反应:N2H4+2H2O2═N2+4H2O.用NA表示阿伏伽德罗常数,下列说法正确的是( )
肼(N2H2)是火箭常用的高能燃料,常温下为液体,其球棍模型如图所示.肼能与双氧水发生反应:N2H4+2H2O2═N2+4H2O.用NA表示阿伏伽德罗常数,下列说法正确的是( )| A. | 标准状况下,11.2LN2中含电子总数为5NA | |
| B. | 标准状况下,22.4LN2H4中所含原子总数为6NA | |
| C. | 标准状况下,3.2gN2H4中含有共价键的总数为0.6NA | |
| D. | 若生成3.6gH2O,则上述反应转移电子的数目为0.2NA |
分析 A、求出氮气的物质的量,然后根据氮气中含14个电子来分析;
B、标况下肼为液体;
C、求出肼的物质的量,然后根据肼中含5条共价键来分析;
D、求出水的物质的量,然后根据反应中当生成4mol水时,转移4mol电子来分析.
解答 解:A、标况下11.2L氮气的物质的量为0.5mol,而氮气中含14个电子,故0.5mol氮气中含7NA个电子,故A错误;
B、标况下肼为液体,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、3.2g肼的物质的量为0.1mol,而肼中含5条共价键,故0.1mol肼中含0.5NA条共价键,故C错误;
D、3.6g水的物质的量为0.2mol,而反应中当生成4mol水时,转移4mol电子,故当生成0.2mol水时,转移0.2NA个电子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


科目:高中化学 来源: 题型:选择题
| A. | 纯银器表面在空气中因化学腐蚀渐渐变暗 | |
| B. | 当镀铜铁制品的镀层破损时,镀层仍能对铁制品起保护作用 | |
| C. | 铁制品长期与氯化铵溶液接触,易发生吸氧腐蚀 | |
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
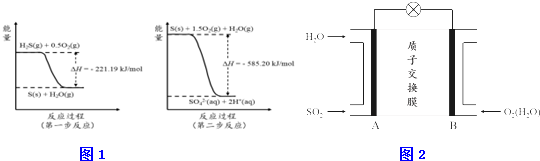
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有NA个氮原子的氮气在标准状况下的体积约为11.2L | |
| B. | 25℃,1.01×105Pa,64g SO2中含有的原子数小于3NA | |
| C. | 在常温常压下,11.2LCl2含有的分子数为0.5NA | |
| D. | 标准状况下,11.2L H2O含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,7.8gNa2S固体和7.8gNa2O2固体中含有的阴离子数目均为0.1NA | |
| B. | 在标准状况下,22.4LCl2和HCl的混合气体中含有的分子总数为2×6.02×1023 | |
| C. | 含1molFeCl3的饱和溶液滴入沸水中得到胶体数目为NA | |
| D. | 标准状况下,1molNa2O2的体积是22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 补血营养品红桃K中添加微量铁粉,作为补铁剂 | |
| B. | 中秋月饼包装袋内有小袋铁粉,作为干燥剂 | |
| C. | 苏打饼干包装盒中有小袋生石灰,作为补钙剂 | |
| D. | 卤制品中加入大量亚硝酸钠,作为保鲜剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种溶液pH的大小顺序是①<②<③ | |
| B. | 若将3种溶液稀释相同倍数,pH变化最大的是③ | |
| C. | 若分别加入25mL0.1 mol•L-1盐酸后,pH最大的是② | |
| D. | 若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植树绿化,美化环境 | B. | 提倡绿色出行,发展公共交通 | ||
| C. | 外出时佩戴防雾霾口罩 | D. | 减少燃煤发电,增加太阳能发电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com