
下列各组分子中,中心原子杂化轨道的类型不相同的是
A.CO2与SO2 B.CH4与NH3 C.SO3与BF3 D. H2S与CCl4
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014四川省资阳市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列递变规律正确的是
A.HClO4、H2SO4、H3PO4的酸性依次增强
B.HCl、HBr 、HI的稳定性依次增强
C.钠、镁、铝的还原性依次减弱
D.N、O、F原子半径逐渐增大
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省绵阳市高三第三次诊断性考试理综化学试卷(解析版) 题型:选择题
20mL0.1mol/LFeCl3溶液中含有部分Fe2+,向其中滴加NaOH溶液至PH=4,溶液中有沉淀生成,过滤,得沉淀和滤液。已知:Ksp [Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)2]=8.0×10-16。
下列说法错误的是
A. 沉淀中只有Fe(OH)3 B. 沉淀中有Fe(OH)3和Fe(OH)2
C. 滤液c(Fe3+)=4.0×10-8mol/L D. 向滤液中滴加FeCl2溶液,无沉淀产生
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省眉山市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列说法正确的是
A.医药中常用酒精消毒是因为酒精能够使细菌蛋白体发生盐析
B.开发清洁能源汽车(如太阳能汽车等)能减少或控制汽车尾气污染
C.目前废旧电池的回收,主要是为了防止电池中NH4Cl对水资源的污染
D.为了防止中秋月饼等富脂食品氧化变质,可在包装袋中放入生石灰
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省攀枝花市高一(下)学期调研检测化学试卷(解析版) 题型:填空题
按要求回答下列问题:
(1) 用电子式表示H2O的形成过程________________________。
(2) 用电子式表示MgCl2的形成过程________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省攀枝花市高一(下)学期调研检测化学试卷(解析版) 题型:选择题
下列关于F、Cl、Br、I的比较,说法正确的是
A.原子最外层的电子数随核电荷数的增加而增多
B.简单阴离子的还原性随核电荷数的增加而增强
C.氢化物的稳定性随核电荷数的增加而增强
D.非金属性随核电荷数的增加而增强
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省攀枝花市高一(下)学期调研检测化学试卷(解析版) 题型:选择题
下列化学用语的书写,正确的是
A.氯气的电子式: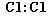 B.硫原子的结构示意图:
B.硫原子的结构示意图: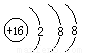
C.溴化钠的电子式: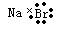 D.质量数为37的氯原子 37 17Cl
D.质量数为37的氯原子 37 17Cl
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市高第二期期末高一化学试卷(解析版) 题型:填空题
工业上用含有铝、铁、铜的废弃合金为主要原料制取硫酸铝溶液、硝酸铜晶体和无水氯化铁,其生产流程如下图所示。
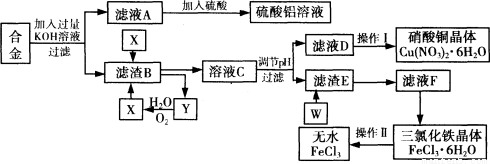
已知:调节适当PH范围可使Fe3+沉淀完全而Cu2+不会沉淀。
请回答下列问题:
(1)写出向合金中加入KOH溶液后所发生反应的离子方程式: 。
(2)在滤液A中直接加入硫酸后所得到的硫酸铝溶液中除含少量硫酸外,还一定含有的杂质是
(填化学式)。
请设计一个更合理的实验方案由滤液A制备纯净的硫酸铝溶液,仿照上图形式画出制备流程图(提示:在箭头上下方标出所用试剂和实验操作) 。
(3) 写出试剂X的名称 。
(4) 实验操作I的顺序依次为 (选填序号)。
A.蒸馏 B.蒸发浓缩 C.过滤 D.冷却结晶
(5) 要制得更纯的Cu(NO3)2·6H2O晶体,必须进行的操作是 (填操作名称)
(6)写出滤渣E与W反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市五校高一下学期期中联考化学试卷(解析版) 题型:简答题
(14分)元素周期表是学习化学的重要工具,它隐含着许多信息和规律,下面是八种短周期元素的相关信息(已知铍的原子半径为0.089nm)
元素代号 | A | B | C | D | E |
原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
F原子中无中子,G最高正价数与负价数相等,且最外层电子数是次外层的二倍,H元素单质焰色反应呈黄色(用相应的元素符号完成下列空白)
(1)B元素在元素周期表中的位置___________________,上述八种元素的最高价氧化物对应的水化物中酸性最强的是__________,A离子的结构示意图_______________。
(2)用电子式表示A、D形成化合物的过程:____________________________________。H、E形成原子个数比为1:1的化合物的电子式为___________,含有的化学键类型为____________。C2D2的电子式为______________________。
(3)下列说法能说明D的非金属性比C强的选项____________
①H2CO4比HDO稳定②HDO4比H2CO4酸性强③C2-比D-易被氧化④HD比H2C稳定⑤铜与HD不反应,但能与浓H2CO4反应⑥铁与D2加热生成FeD3,铁与C加热生成FeC⑦C原子与D原子电子层数相同,D原子半径小于C原子。
A、全部 B、②③④⑥⑦ C、①②④⑤⑥ D、除①以外
(4)A、B、C、D、E形成的简单离子半径由大到小的顺序为_______________________。(用具体离子符号表示)
(5)C单质与H的最高价氧化物对应水化物在加热条件下能发生反应,若有3mol的C参与反应,转移4NA的电子,请写出离子反应方程_______________________________________,氧化剂与还原剂的质量之比_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com