
| ||
| ||


科目:高中化学 来源: 题型:
| A、一定温度下,压缩容器体积,则正反应速率加快,逆反应速率减慢 | ||
| B、若甲醇的生成速率等于一氧化碳的消耗速率,则该反应达到平衡状态 | ||
C、升高温度,重新达到平衡时,
| ||
| D、使用催化剂,反应的平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2SO3和HNO3 |
| B、Na2SO3和H2SO4 |
| C、Na2S和H2SO4 |
| D、Na2S和HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
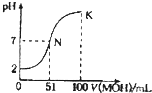 常温下,向l00mL 0.01mol?L-1HA溶液中逐滴加入0.02mol??L-1MOH溶液,如图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中,正确的是( )
常温下,向l00mL 0.01mol?L-1HA溶液中逐滴加入0.02mol??L-1MOH溶液,如图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中,正确的是( )| A、HA为一元强酸,MOH为一元强碱 |
| B、K点所示溶液中c(A-)>c(M+) |
| C、N点水的电离程度小于K点水的电离程度 |
| D、K点对应的溶液的pH=10,则有c(MOH)+c(OH-)-c(H+)=0.005mol??L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
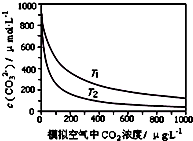 大气中CO2含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境.某研究小组在实验室测得不同温度下(T1,T2)海水中CO32-浓度与模拟空气中CO2浓度的关系曲线.下列说法不正确的是( )
大气中CO2含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境.某研究小组在实验室测得不同温度下(T1,T2)海水中CO32-浓度与模拟空气中CO2浓度的关系曲线.下列说法不正确的是( )| A、T1>T2 |
| B、海水温度一定时,大气中CO2浓度增加,海水中溶解的CO2随之增大,导致CO32-浓度降低 |
| C、当大气中CO2浓度确定时,海水温度越高,CO32-浓度越低 |
| D、大气中CO2含量增加时,海水中的珊瑚礁将逐渐溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com