
有铝和四氧化三铁组成的铝热剂粉末,在隔绝空气中的条件下引燃,使之充分反应,把所得混合物研细,并分成两等份,分别投入到过量烧碱溶液和盐酸中,充分反应后,前者消耗氢氧化钠mmol,放出标准状况下的气体0.672L;后者消耗盐酸nmol,放出标准状况下气体VL。若将等质量的这种铝热剂中的铝粉和足量的稀硫酸反应,可以得到标准状况下的气体6.72L。
(1)铝热剂中各成分的质量分数。
(2)m、n、V的值各是多少?
(1)![]()
Fe3O4%=1-27.95%=72.05%
(2) m=0.10(mol)
N =0.48(mol)
V =2.688(L)
题目没有指明铝热剂中铝粉和四氧化三铁各自的质量分数,那么铝粉和四氧化三铁混合有三种情况:①铝粉和四氧化三铁适量,恰好两者完全反应,反应物无剩余,产物是三氧化二铝和单质铁,该混合物投入过量的氢氧化钠溶液中,铁跟氢氧化钠溶液不反应,三氧化二铝跟氢氧化钠溶液反应,但是不放出气体,不合题意;②铝热剂中四氧化二铁过量,反应后的混合物中有三氧化二铝、铁和剩余的四氧化三铁,将其混合物投入过量的氢氧化钠溶液中,铁和四氧化三铁跟氢氧化钠溶液都不反应,三氧化二铝跟氢氧化钠反应,但是不放出气体,不合题意;③铝热剂中铝粉过量,反应后混合物中有三氧化二铝和剩余的铝,将其混合物投入过量的氢氧化钠溶液中,铁跟氢氧化钠不反应,三氧化二铝和铝都能跟氢氧化钠溶液反应,而且铝在反应时能够放出氢气,符合题意。
(1)求铝热剂中各成分的质量分数。
设原铝热剂中含xg。
2Al+3H2SO4=Al2(SO4)3+3H2↑
2×27g 3×22.4L
xg 6.72L
2×7∶x=3×22.4∶6.72
解得x=5.4(g)
设铝热反应后剩余的铝为yg。
2Al+2NaOH=2H2O=2NaAlO2+3H2↑
2×27g 3×22.4L
yg 0.672L
2×27∶y=3×22.4∶0.672
解得 y=0.54(g)
故参加铝热反应的铝粉为5.4-0.54×2=4.32(g)
设铝热剂中四氧化三铁的质量为zg
8Al + 3Fe3O4 → 4Al2O3 + 9Fe
8×27g 3×232 4mol 9mol
4.32g zg b=0.08mol c=0.18mol
8×27∶4.32=3×232∶z
解得z=13.92(g)
![]()
Fe3O4%=1-27.95%=72.05%
(2)求m、n和V
反应后每份反应后的混合物含铝0.54g,含铁0.18/2=0.09(mol)含三氧化二铝0.08/2=0.04(mol)
Al2O3 + 2NaOH=2NaAlO2+H2O
1mol 2mol
0.04mol 0.08mol
所以m=0.02+0.08=0.10(mol)
2Al + 6HCl = 2AlCl3 + 3H2↑
2×27g 6mol 3×22.4L
0.54g 0.06mol 0.672L
Fe + 2HCl = FeCl2 + H2↑
1mol 2mol 22.4L
0.09mol 0.18mol 22.4×0.09L
Al2O3 + 6HCl=2AlCl3+3H2O
1mol 6mol
0.04mol 6×0.04mol
所以n=0.06+0.18+0.24=0.48(mol)
V=0.672+22.4×0.09=2.688(L)
|


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:038
有铝粉和四氧化三铁组成的铝热剂,在隔绝空气的条件下灼烧,使之充分反应。将所得混合物研细并分成两等份,分别投入过量的烧碱溶液和盐酸中。充分反应后,前者捎耗mmol NaOH,放出气体0.336 L;后者消耗nmolHCI,放出气体VL。若将等 质量的这种铝热剂中的铝粉与足量的稀硫酸作用,可得3.36L气体(气体体积均在标 准状况下测定)。求:
(1)该铝热剂的质量分数。
(2)m、n、y的值。
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:038
(1)该铝热剂的质量分数。
(2)m、n、y的值。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)该铝热剂的组成成分的质量分数。
(2)m、n、V的值。
查看答案和解析>>
科目:高中化学 来源: 题型:
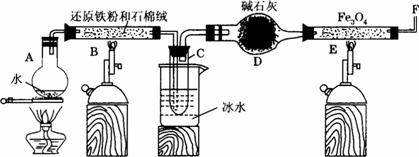
(1)为防止A中液体暴沸,可以采取的措施是___________;装置D能否改用盛有浓硫酸的洗气瓶___________。
(2)反应3Fe+4H2O(g)====Fe3O4+4H2↑在一定条件下实际为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释__________________________________。
(3)停止反应,待B管冷却后,取其中固体加入过量稀盐酸,充分反应后过滤。简述证明滤液中含有Fe3+的实验操作及现象_____________________________________________________。
(4)若E管中反应按以下两步进行:Fe3O4+H2====3FeO+H2O,FeO+H2====Fe+H2O,假设实验开始时E管中的Fe3O4为23.
①Fe ②Fe租Fe3O4 ③FeO和Fe3O4 ④Fe和FeO ⑤Fe、FeO和Fe3O4
用此20 g固体与铝粉在一定条件下进行铝热反应,最多可消耗铝粉_________g(不考虑空气中的成分参与反应)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com