
下列不能由单质直接通过化合反应制取的是()
①FeCl2 ②FeCl3③FeS ④Mg3N2 ⑤CuS ⑥Al2S3 ⑦AlCl3.
A. ①③ B. ①④ C. ①⑤ D. ①⑥
考点: 铁的化学性质;镁的化学性质;铝的化学性质.
专题: 元素及其化合物.
分析: ①根据铁与氯气反应的产物分析;
②根据铁与氯气反应的产物分析;
③根据铁粉和硫粉混合加热即生成硫化亚铁分析;
④根据镁和氮气反应生成氮化镁分析;
⑤根据铜和硫粉混合加热即生成硫化亚铜分析;
⑥根据铝和硫反应生成硫化铝进行分析;
⑦根据Al与氯气在点燃时能直接化合生成AlCl3分析;
解答: 解:①氯气具有强氧化性,和变价金属只生成高价金属氯化物,Fe在Cl2中燃烧只生成FeCl3,单质间反应不能生成FeCl2,故①选;
②FeCl3可由Fe在Cl2中燃烧生成,故②不选;
③硫具有弱氧化性,和变价金属只生成低价金属氯化物,铁粉和硫粉混合加热即生成硫化亚铁,故③不选;
④镁和氮气反应3Mg+N2 Mg3N2,故④不选;
Mg3N2,故④不选;
⑤硫的氧化性弱,和金属反应生成低价态的金属硫化物,铜和硫粉反应Cu+S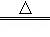 Cu2S,不能通过单质之间的反应直接制取CuS,故⑤选;
Cu2S,不能通过单质之间的反应直接制取CuS,故⑤选;
⑥铝和硫反应2Al+3S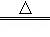 Al2S3,故⑥不选;
Al2S3,故⑥不选;
⑦Al与氯气反应3Cl2+2Al 2AlCl3,故⑦不选;
2AlCl3,故⑦不选;
故选C.
点评: 本题考查常见金属和非金属的性质,熟练掌握常铁、铝、硫、氯气、氧气等物质的化学性质是解答的关键,题目难度不大,注意基础知识的积累.


科目:高中化学 来源: 题型:
下列叙述中错误的是( )
A.带相反电荷离子之间的相互吸引称为离子键
B.金属元素与非金属元素化合时,不一定形成离子键
C.某元素的原子最外层只有一个电子,它跟卤素原子结合时所形成的化学键不一定是离子键
D.非金属原子之间不可能形成离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
鉴别FeCl3溶液和Fe(OH)3胶体,下列方法中最简单有效的是()
A. 加入足量的盐酸 B. 加热煮沸
C. 加入足量的NaOH溶液 D. 观察能否产生丁达尔现象
查看答案和解析>>
科目:高中化学 来源: 题型:
已知HI为无色气体,对于可逆反应H2(g)+I2(g)═2HI(g),下列叙述能够说明反应已达到平衡状态的是()
A. 混合气体的颜色不再变化
B. υ(H2)正=υ(HI)逆
C. 断裂2mol H﹣I键的同时生成1mol I﹣I键
D. H2、I2、HI的物质的量浓度之比为1:1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
把Ba(OH)2溶液滴入到明矾溶液中,使SO42﹣全部转化成BaSO4沉淀,此时铝元素的主要存在形式是()
A. Al3+ B. Al(OH)3 C. AlO2﹣ D. Al3+和Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
把铝粉和Fe3O4粉末配成铝热剂并分成两份,第一份在高温下恰好完全反应,然后将生成物与足量盐酸充分反应;第二份直接加入足量的氢氧化钠溶液使之充分反应,前后两种情况下生成的气体在相同状况下的体积比是()
A. 3:4 B. 4:3 C. 3:8 D. 8:3
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下,下列叙述正确的是()
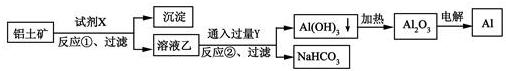
A. 试剂X可以是氢氧化钠溶液,也可以是盐酸
B. 反应①、过滤后所得沉淀为氢氧化铁
C. 图中所示转化反应都不是氧化还原反应
D. 反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
NA为阿伏加德罗常数,下列说法正确的是()
A. 标准状况下,11.2 L的戊烷所含的分子0.5NA
B. 28 g乙烯所含共用电子对数目为4NA
C. 标准状况下,11.2 L二氯甲烷所含分子数为0.5 NA
D. 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列指定反应的离子方程式正确的是 ( )
A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B.Na2CO3溶液中CO32-的水解:CO32-+H2O=HCO3-+OH-
C.酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+=I2+3H2O
D.NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com