
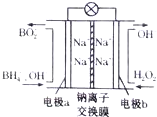
 �ݱ����������⻯����NaBH4��BԪ�صĻ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ��为�����ϲ���Pt/C���������ϲ���MnO2���������վ�ͨ�����ǵ�Դ���乤��ԭ����ͼ��ʾ������˵����ȷ���ǣ�������
�ݱ����������⻯����NaBH4��BԪ�صĻ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ��为�����ϲ���Pt/C���������ϲ���MnO2���������վ�ͨ�����ǵ�Դ���乤��ԭ����ͼ��ʾ������˵����ȷ���ǣ�������| A�� | �õ�صĸ�����ӦΪBH4-+8OH--8e-�TBO2-+6H2O | |
| B�� | ��طŵ�ʱNa+��b��������a���� | |
| C�� | ÿ����3mol H2O2��ת�Ƶĵ���Ϊ3mol | |
| D�� | �缫a����Mn02���缫���� |
���� ����ͼƬ֪��˫��ˮ�õ��ӷ�����ԭ��Ӧ����b�缫Ϊ������a�缫Ϊ������������BH4-�õ��Ӻ����������ӷ�Ӧ����BO2-��
A��������BH4-�õ��Ӻ����������ӷ�Ӧ����BO2-��
B��ԭ��طŵ�ʱ���������Һ���������������ƶ���
C��˫��ˮ�õ��ӷ�����ԭ��Ӧ����b�缫Ϊ������a�缫Ϊ������
D������ת�Ƶ��Ӻ�˫��ˮ֮��Ĺ�ϵʽ���㣮
��� �⣺A����������������Ӧ����BO2-���缫��ӦʽΪBH4-+8OH--8e-=BO2-+6H2O����A��ȷ��
B��ԭ��ع���ʱ���������������ƶ������������ƶ�����Na+��a��������b��������B����
C�������缫��ӦʽΪH2O2+2e-=2OH-��ÿ����3molH2O2��ת�Ƶĵ���Ϊ6mol����C����
D���缫b����MnO2���缫���ϣ�Ϊ��������D����
��ѡA��
���� ���⿼��ԭ��ع���ԭ�����漰�缫�ж���缫��Ӧʽ��д�����⣬����ʱע���������ԭ�ĽǶ��ж�ԭ��ص��������Լ��缫����ʽ����д���������ѵ���״���Ϊ�缫����ʽ����д��ע�⻯�ϼ۵ı仯��


 ����������ϵ�д�
����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
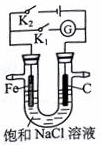
| A�� | K1�պϣ���������������K3[Fe��CN��6]��Һ��������Ѫ��ɫ���� | |
| B�� | K2�պϣ�����������ʯī���������������� | |
| C�� | K2�պϣ�̼���Ϸ�����ԭ��Ӧ�������ɻ���ɫ���� | |
| D�� | ��U��֧�ܷ�ղ��պ�K1һ��ʱ���U�����Ҳ�Һ���������Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����¶ȣ��ٽ�CO32-ˮ�⣬pH��С | |
| B�� | ����Ũ�ȣ�c��Na+��=2[c��CO32-��+c��HCO3-��+c��H2CO3��] | |
| C�� | ����Ũ�ȣ�c��Na+��+c��H+��=c��HCO3-��+c��CO32-��+c��OH-�� | |
| D�� | ����Ũ�ȣ�c��Na+����c��CO32-����c��OH-����c��H+����c��HCO3-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 +Br2
+Br2
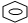 +HO-NO2
+HO-NO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
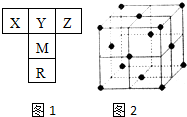 ��ͼ1��Ԫ�����ڱ���һ���֣���֪R�ĺ˵����С��36����̬�⻯��е㣺MHn��YHn��
��ͼ1��Ԫ�����ڱ���һ���֣���֪R�ĺ˵����С��36����̬�⻯��е㣺MHn��YHn��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
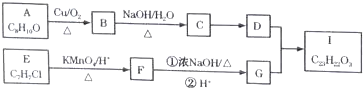
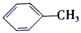 $��_{��}^{KMnO_{4}/H+}$
$��_{��}^{KMnO_{4}/H+}$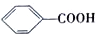
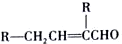
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ߴ��ȵĵ��������������̫���ܵ�ذ���ά | |
| B�� | ʯ�Ϳ���ͨ���ѽ⡢�ѻ��������仯�����Ҫ����ԭ����ϩ | |
| C�� | ������͵�����Һ�����ڽ��壬��������ͭ��Һ���Է�������۳� | |
| D�� | ֲ���������ں���̼̼˫��������ڿ����г�ʱ����������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ����I | ����II |
| A | ��֬�����Ͷ����� | һ�������¶��ܷ���������Ӧ |
| B | CuSO4����������Ӿ�������� | ͭ����ʹ�����ʱ��� |
| C | ���ǡ����ۡ���ά���ǻ�ԭ���� | ����һ�������¶��ܷ���������Ӧ |
| D | �����ʽṹ�д����ļ� | �������ܱ��ֳ����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵ������������������ֱ���ȫȼ�գ����߷ų������� | |
| B�� | ��ϡ��Һ�У�H+��aq��+OH-��aq���TH2O��l������H=-57.3 kJ/mol��������0.5 mol H2SO4��Ũ�����뺬1 mol NaOH����Һ��ϣ��ų�����������57.3 kJ | |
| C�� | ��C��ʯī��=C�����ʯ����H=+1.90 kJ/mol��֪ʯī�Ƚ��ʯ�ȶ� | |
| D�� | ��101 kPaʱ��2 g H2 ��ȫȼ������Һ̬ˮ���ų�285.8 kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2��g��+O2��g���T2H2O��g����H=-571.6kJ/mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com