
【题目】下列“试剂”和“试管中的物质”不能完成“实验目的”的是( )
实验目的 | 试剂 | 试管中的物质 | |
A | 羟基对苯环的活性有影响 | 饱和溴水 | ①苯 ②苯酚溶液 |
B | 甲基对苯环的活性有影响 | 酸性KMnO4溶液 | ①苯 ②甲苯 |
C | 苯分子中没有碳碳双键 | Br2的CCl4溶液 | ①苯 ②己烯 |
D | 碳酸的酸性比苯酚强 | 石蕊溶液 | ①苯酚溶液 ②碳酸溶液 |
A.AB.BC.CD.D
【答案】B
【解析】
A. 饱和溴水不能与苯发生苯环上的取代反应,但能与苯酚发生苯环上的取代反应生成白色沉淀,故本方案能证明羟基对苯环的活性有影响,即可完成实验目的,A选项不符合题意;
B. 酸性KMnO4溶液不能与苯反应,能将甲苯的氧化,但甲苯被氧化的部位是甲基而非苯环,反映的是苯环对甲基的影响,而非甲基对苯环的影响,即本方案不能完成实验目的,B选项符合题意;
C. 碳碳双键能使Br2的CCl4溶液褪色,苯不能使Br2的CCl4溶液褪色,可以证明苯分子中没有碳碳双键,即本方案可完成实验目的,C选项不符合题意;
D.碳酸溶液能使石蕊溶液变红,而苯酚溶液不能使石蕊溶液变红,所以本方案可完成实验目的, D选项不符合题意;
答案选B。


科目:高中化学 来源: 题型:
【题目】对于下列化学平衡在一定条件下发生移动的描述,不正确的是
A. Cl2+H2O![]() HCl+HClO,氯水中加入碳酸钙,漂白性增强
HCl+HClO,氯水中加入碳酸钙,漂白性增强
B. ZnS + Cu2+![]() CuS + Zn2+,闪锌矿(ZnS)遇CuSO4溶液转化为铜蓝(CuS)
CuS + Zn2+,闪锌矿(ZnS)遇CuSO4溶液转化为铜蓝(CuS)
C. 2NO2![]() N2O4 ΔH<0,将装有NO2的玻璃球浸入热水中,红棕色变浅
N2O4 ΔH<0,将装有NO2的玻璃球浸入热水中,红棕色变浅
D. Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色) +2H+,K2Cr2O7溶液中滴加几滴浓硫酸,橙色加深
2CrO42-(黄色) +2H+,K2Cr2O7溶液中滴加几滴浓硫酸,橙色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷在加热条件下可还原氧化铜,气体产物除水蒸气外,还有碳的氧化物,某化学小组利用如图装置探究其反应产物。

查阅资料:
①CO能与银氨溶液反应:CO+2Ag(NH3)2++2OH-=2Ag↓+2NH4++CO32-+2NH3
②Cu2O为红色,不与Ag反应,发生反应:Cu2O+2H+=Cu2++Cu+H2O
③已知Al4C3与CaC2类似易水解,CaC2的水解方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑
(1)装置A中反应的化学方程式为___。
(2)装置F的作用为___;装置B的名称为___。
(3)按气流方向各装置从左到右的连接顺序为A→__。(填装置名称对应字母,每个装置限用一次)
(4)实验中若将A中分液漏斗换成![]() (恒压漏斗)更好,其原因是___。
(恒压漏斗)更好,其原因是___。
(5)装置D中可能观察到的现象是___。
(6)当反应结束后,装置D处试管中固体全部变为红色。设计实验证明红色固体中含有Cu2O(简述操作过程及现象):__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,硫酸与 NaOH 溶液相互滴定的滴定曲线如图所示。下列有关叙述不正确的 是( )
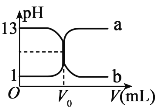
A.曲线 a 是用 NaOH 溶液滴定硫酸的滴定曲线
B.曲线 a 和曲线 b 滴定过程中均存在:c(H+)+c(Na+)=c(OH-)+2c(SO42-)
C.用 NaOH 溶液滴定硫酸溶液时可用酚酞作指示剂
D.等体积的硫酸与 NaOH 溶液分别与等质量铝粉反 应生成 H2 的质量比一定为 1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】杯环芳烃因其结构类似于酒杯而得名,其键线式如图,下列关于杯环芳烃的说法正确的是( )
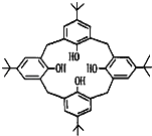
A.属于芳香烃B.最多与6mol H2发生加成反应
C.分子式为C44H56O4D.分子内所有原子一定在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO、H2 是重要的工业原料,在高温、催化剂存在的条件下,可用甲烷 和水蒸气为原料制取它:CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH0
CO(g)+3H2(g) ΔH0
(1)已知:
① 2H2(g)+O2(g)=2H2O(g) ΔH1=-484kJ·mol-1
② CH4(g)+1.5O2(g)=CO(g)+2H2O(g) ΔH2=-564kJ·mol-1。
则ΔH0 =_____。
(2)一定温度下,将一定量甲烷与水蒸气的混合气体置于某密闭容器中发生反应 生成 CO、H2,测得反应体系中平衡时的某种量值 X 与温度(T)、压强(P)之间的关系如图 所示:
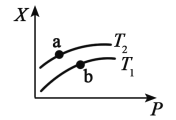
若 X 表示 CH4 的百分含量,则 T1_________T2(填“>”“<”“无法确定”,下同),X 还可 以表示_____(在下列选项中选填序号),a、b 两点的平衡常数 K(a) ____K(b)。
A.混合气体的平均摩尔质量 B.CO 的产率 C.ΔH 值
(3)若在 T3 时将 4mol H2O(g)与 a mol CH4 置于 2L 恒容密闭容器中,测得 CO 的 浓度(mol/L)与时间 t(min)的关系如图 所示。
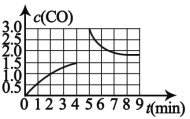
①反应 4min 后达平衡, 反应 4min 内用 H2浓度变化表示的反应速率 v(H2)=__________________
②若在第 5 分钟时改变条件,CO 浓度变化曲线如图 所示,则改变条件可能是____________
(4)从焓变角度上看,反应 CO2(g)+H2O(g)=CO(g)+H2(g)+O2(g)_____(填“具 有”或“不具有”)自发性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】GaN是制造5G芯片的材料,氮化镓铝和氮化铝LED可发出紫外光。回答下列问题:
(1)基态As原子核外电子排布式为[Ar]________,下列状态的铝中,电离最外层的一个电子所需能量最小的是_____________(填标号)。
A. ![]() B.
B. ![]() C.[Ne] D.
C.[Ne] D. ![]()
(2)8—羟基喹啉铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与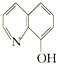 (8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为_______;
(8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为_______; 所含元素中电负性最大的是___(填元素符号),C、N、O的杂化方式依次为 _____、_________和____________。
所含元素中电负性最大的是___(填元素符号),C、N、O的杂化方式依次为 _____、_________和____________。
(3)已知下列化合物的熔点:
化合物 | AlF3 | GaF3 | AlCl3 |
熔点/℃ | 1040 | 1000 | 194 |
①表中卤化物的熔点产生差异的原因是____________。
②熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6,二聚体Al2Cl6的结构式为_______;其中Al的配位数为_________。
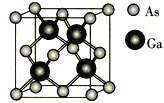
(4)GaAs的晶胞结构如图所示,紧邻的As原子之间的距离为x,紧邻的As、Ga原子之间的距离为y,则![]() =________。
=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向20mL0.2mol·L-1NaCN溶液中加入0.2mol·L-1的盐酸,溶液pH随所加盐酸体积的变化如图所示(M>7)。下列说法不正确的是
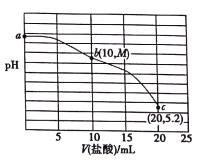
A. 25℃时,K(HCN)≈10-9.4
B. b点时,c(CN-)<c(HCN)
C. c点时,c(Cl-)>c(H+)+c(HCN)
D. a、b、c三点时,水的电离程度:a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
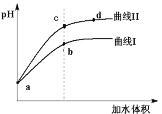
【题目】已知T ℃时两种弱酸的电离平衡常数如下表。将pH和体积均相同的两种酸溶液M、N分别稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
弱酸 | HNO2 | CH3COOH |
电离平衡常数 | 5.0×10-4 | 1.7×10-5 |
A.曲线Ⅰ代表CH3COOH溶液
B.M、N两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
C.溶液中水的电离程度:b点<c点
D.从c点到d点,溶液中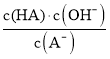 保持不变(其中HA、A-分别代表相应的酸和酸根离子)
保持不变(其中HA、A-分别代表相应的酸和酸根离子)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com