
��һ�������£���E(g)��F(g)������������2 L�ܱ������У�����������Ӧ������5 minĩ�ﵽƽ�⣺2E(g)��F(g) 2G(g)���й��������£�
2G(g)���й��������£�
| | E��g�� | F��g�� | G��g�� |
| ��ʼŨ�ȣ�mol?L-1�� | 2.0 | 1.0 | 0 |
| ƽ��Ũ�ȣ�mol?L-1�� | c1 | c2 | 0.4 |
D
�������������A����Ӧ��ǰ5min�ڣ������������ͼ��������c1=1.6mol/L��c2=0.2mol/L��E�����ʵ���Ũ�ȱ仯Ϊ0.4 mol/L����Ӧ����v��E��=��c/��t=0.02mol/��L?min��������B�����ֻ������������ʷ�Ӧ������һ�ֵ�Ũ�Ȼ������һ�ַ�Ӧ���ת���ʣ�������ת���ʼ�С�������������䣬������E��Ũ�ȣ����ƽ��ʱE��ת���ʻ��С������C�������¶ȣ�E���ʵ�����С��˵��ƽ��������У�����ӦΪ���ȷ�Ӧ����H��0������D����ʼ��ΪEΪ4mol��FΪ2mol��ƽ�������2.0mol E��1.0mol F���൱����ʼ�����룬ѹǿ��Сƽ��������У�G��Ũ��С��0.2mol/L����ȷ��
���㣺���黯ѧ��Ӧ���ʺͻ�ѧƽ��ļ��㼰Ӱ�����ء�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����β���е��ж�����NO��CO����һ�������¿ɷ�����Ӧ����N2��CO2�����й��ڴ˷�Ӧ��˵���У���ȷ����( )
| A����Сѹǿ������Ӧ���� | B������ѹǿ�ܼ�С��Ӧ���� |
| C��ʹ���ʵ��Ĵ���������Ӧ���� | D�������¶ȶԷ�Ӧ������Ӱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��������a��b����п���У��ֱ���������ҵ�����ϡH2SO4��ͬʱ��a�м���������CuSO4��Һ����ͼ��ʾ����H2�������V����ʱ�䣨t���Ĺ�ϵ��������ȷ���ǣ� ��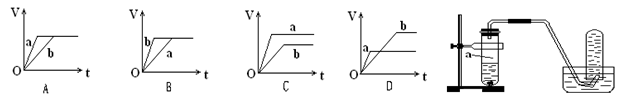
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ�������£�ˮ���������淴Ӧʱ��ı仯���Ʒ�����ͼ����( )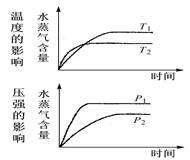
A��CO2(g)+2NH3( g) CO(NH2)2(s)+H2O(g); ��H<0 CO(NH2)2(s)+H2O(g); ��H<0 |
B��CO2(g)+ H2(g)  CO(g)+H2O(g); ��H>0 CO(g)+H2O(g); ��H>0 |
C��CH3CH2OH CH2=CH2(g)+ H2O(g); ��H>0 CH2=CH2(g)+ H2O(g); ��H>0 |
D��2C6H5CH2CH3(g)+O2(g) 2C6H-5CH=CH2(g)+2H2O(g); ��H<0 2C6H-5CH=CH2(g)+2H2O(g); ��H<0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������Ƭ��l00 mL 0.01 mol��L��ϡ���ᷴӦ����Ӧ����̫����Ϊ�˼ӿ�˷�Ӧ���ʶ����ı�H2�IJ���������ʹ�����·����е�
�ټ�H2O �ڼ�KNO3��Һ �۵��뼸��Ũ���� �ܼ����������� �ݼ�NaCl��Һ
���뼸������ͭ��Һ �������¶�(����������ӷ�) �����10 mL 0.1 mol��L����
| A���٢ޢ� | B���ۢݢ� | C���ۢߢ� | D���ۢܢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����ȼ�ϵ����Ŀǰ��Ϊ�����ȼ�ϵ��֮һ���������ɼ���Ӧԭ����ͼ��ʾ��
����˵������ȷ����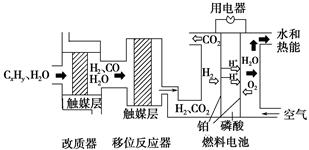
| A����ϵͳ��ֻ���ڻ�ѧ�ܺ͵��ܵ��ת�� |
B������λ��Ӧ���У���ӦCO(g)��H2O(g) 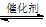 CO2(g)��H2(g)����H��0�������¶�Խ�ߣ���v(CO)Խ�� CO2(g)��H2(g)����H��0�������¶�Խ�ߣ���v(CO)Խ�� |
| C������������λ��Ӧ���������ǽ�CxHyת��ΪH2��CO2 |
| D���õ�������ĵ缫��ӦΪO2��4H����4e��=2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�������ʶ���������Ʒ�Ӧ�ų�H2������H2������������ȷ����
��C2H5OH ��NaOH��Һ �۴�����Һ
| A���۩��ک��� | B���ک��٩��� | C���٩��ک��� | D���۩��٩��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ���¶��£����淴ӦA(��)��3B(��)  2C(��)�ﵽƽ��ı�־��
2C(��)�ﵽƽ��ı�־��
A��A��B��C�ķ�������Ϊ1:3:2
B��A��B��C��Ũ�����
C��C���ɵ�������C�ֽ���������
D����λʱ������n mol A��ͬʱ����3n mol B
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ�������£����淴ӦX(g) + 3Y(g) 2Z(g)����X��Y��Z��ʼŨ�ȷֱ�Ϊc1��c2��c3������Ϊ0����λmol/L��������ƽ��ʱX��Y��Z��Ũ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.08mol/L���������жϲ���������
2Z(g)����X��Y��Z��ʼŨ�ȷֱ�Ϊc1��c2��c3������Ϊ0����λmol/L��������ƽ��ʱX��Y��Z��Ũ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.08mol/L���������жϲ���������
| A��c1:c2 = 1:3 | B��ƽ��ʱ��Y��Z����������֮��Ϊ3:2 |
| C��X��Y��ת���ʲ���� | D��c1��ȡֵ��ΧΪ0 < c1 < 0.14mol/L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com