
【题目】某原电池总反应的离子方程式为2Fe3++Fe=3Fe2+,以下不能实现该反应的原电池是( )
A.正极为Cu,负极为Fe,电解质溶液为FeCl3
B.正极为C,负极为Fe,电解质溶液为Fe(NO3)3
C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3
D.正极为Ag,负极为Fe,电解质溶液为Fe2(SO4)3
科目:高中化学 来源: 题型:
【题目】有人分析一些小而可溶的有机分子样品时,发现它们含有碳、氢、氧、氮等元素,这些样品很可能是( )
A. 脂肪 B. 氨基酸
C. 葡萄糖 D. 油类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铈(58Ce)常用于制作稀土磁性材料,可应用于制造玻璃、打火石、陶瓷和合金等。已知:Ce4++Fe2+=Ce3++Fe3+。下列说法正确的是( )
A. Ce元素位于元素周期表第六周期第IIIB族
B. ![]() 、
、![]() 是同素异形体
是同素异形体
C. 铈能溶于HI溶液,发生反应的离子方程式为:Ce+4H+=Ce4++2H2
D. 铈的原子核外有58个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氟酸是一种弱酸,可用来刻蚀玻璃。
已知25℃时:①HF(aq)+OH-(aq)=F-(aq)+H2O(1)ΔH=-67.7kJ·mol-1,②H+(aq)+OH-(aq)=H2O(1) ΔH=-57.3kJ·mol-1。在20mL0.1mol·L-1氢氟酸中加入VmL0.1mol·L-1NaOH溶液,下列有关说法不正确的是
A. 氢氟酸的电离方程式及热效应可表示为: HF(aq)![]() F-(aq)+ H+(aq) ΔH=-10.4kJ·mol-1
F-(aq)+ H+(aq) ΔH=-10.4kJ·mol-1
B. 当V=20时,溶液中:c(OH-)=c(HF)+c(H+)
C. 当V=20时,溶液中:c(F-)<c(Na+)=0.1mol·L-1
D. 当V>0时,溶液中可能存在:c(Na+)>c(F-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象或图象信息不能充分说明相应化学反应是放热反应的是( )
A | B | C | D | |
反应装置图或图象 |
|
|
|
|
实验现象 | 温度计的水银柱不断上升 | 反应物总能量大于生成物总能量 | 反应开始后,甲处液面低于乙处液面 | 反应开始后,针筒活塞向右移动 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据ETH天文研究所报告,组成太阳的气体中存在20Ne和22Ne,下列关于20Ne和22Ne的说法正确的是( )
A.20Ne和22Ne互为同位素
B.20Ne和22Ne互为同分异构体
C.20Ne和22Ne的质量数相同
D.20Ne和22Ne的中子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图是元素周期表的一部分,请回答下列问题。
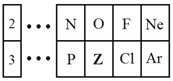
(1)Z元素在元素周期表中位于第________族。
(2)Z的原子半径__________(填“大于”、“小于”或“等于”)Si的原子半径。
(3)Cl元素的非金属性比Z元素的__________(填“强”或“弱”)。
(4)Z元素的气态氢化物的化学式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将两种不同物质的量浓度的Na2CO3溶液升高温度溶液中c(CO32-)变化如图所示,下列微粒的物质的量浓度关系正确的是( )
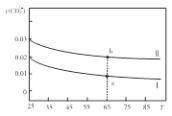
A.将溶液I升高温度,溶液pH减小
B.溶液a比溶液b中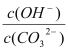 更大
更大
C.65℃时,向溶液a中加入1.06gNa2CO3固体,溶解后即为溶液b
D.溶液II一定存在:c(Na+)=2c(CO32-)+c(HCO3-)+c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com