
实验室可用如图所示的装置进行CO和CO2混合气体的分离和干燥。已知a为止水夹,b为分液漏斗丙的活塞,可供选用的试剂有NaHCO3溶液、NaOH溶液、NaHS溶液、浓硫酸、无水氯化钙、稀硫酸。试填空回答:

(1)广口瓶甲中应放的试剂为________,广口瓶乙中应放的试剂为________,分液漏斗丙中应放的试剂为________。
(2)第一步应先分离出________,分离时应先关闭________。打开________,发生反应的离子方程式为___________________________________________
__________________。
(3)第二步分离出________时,先关闭________,打开________,发生反应的离子方程式为_____________________________________________________
___________________。
科目:高中化学 来源: 题型:
下列各组原子中,彼此化学性质一定相似的是( )
A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子
C.2p轨道上只有2个电子的X原子与3p轨道上只有2个电子的Y 原子
原子
D.最 外层都只有一个电子的X、Y原子
外层都只有一个电子的X、Y原子
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组同学以碳棒为电极电解CuCl2溶液时,发现阴极碳棒上除了有红色物质析出外,还有少量白色物质析出。为探究阴极碳棒上的产物,同学们设计了如下实验过程。
(1)对比实验(以碳棒为电极电解下列溶液)
| 电解质溶液 | 阴极析出物质 | |
| 实验1 | CuSO4溶液 | 红色固体 |
| 实验2 | CuSO4和NaCl的混合溶液 | 红色固体和少量白色固体 |
(2)提出假设
①红色物质一定有铜,还可能有Cu2O;
②白色物质为铜的化合物,其化学式可能为________。
(3)实验验证
取电解CuCl2溶液后的阴极碳棒,洗涤、干燥。连接下列装置进行实验,验证阴极产物。
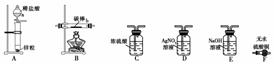
仪器a的名称为________,各装置从左至右的连接顺序为________。
(4)观察现象,得出结论
实验结束后,碳棒上的白色物质变为红色,F中物质不变色,D中出现白色沉淀。
根据现象写出装置B中发生反应的化学方程式:
________________________________________________________________________。
(5)问题讨论
①欲洗去碳棒上的红色和白色物质,可将碳棒插入稀硝酸中,则红色物质消失的离子方程式为______________________;白色物质消失的离子方程式为_________________
______________________。
②实验过程中,若装置B中的空气没有排净就开始加热,可能对实验造成的影响是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组溶液中,用括号内的试剂及物质间相互反应不能鉴别的一组是
( )
A.Ba(OH)2、KSCN、NaCl、Mg(NO3)2(FeCl3溶液)
B.NaNO3、NaHCO3、(NH4)2SO3、Na2SiO3(H2SO4溶液)
C.NH4Br、K2CO3、NaI、CaCl2(AgNO3溶液)
D.(NH4)3PO4、NaBr、CuSO4、AlCl3(KOH溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知具有碳碳双键结构的有机物可被碱性高锰酸钾溶液氧化成二元醇,如H2C===CH2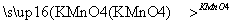 HOCH2CH2OH。现以CH2===C(CH3)2为原料按下列方式合成环状化合物D和高分子化合物G。
HOCH2CH2OH。现以CH2===C(CH3)2为原料按下列方式合成环状化合物D和高分子化合物G。
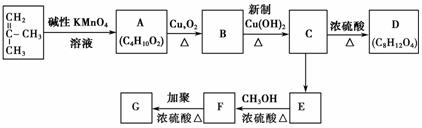
(1)A→B的反应类型是________,C→E的反应类型是________,E→F的反应类型是________。
(2)D的结构简式是________,G的结构简式是________。
(3)B→C的化学方程式是________________________________________________________________________。
(4)E→F的化学方程式是________________________________________________________________________。
(5)C物质的同分异构体中,与C所含官能团种类和数目都相同的同分异构体有________种(不包括C)。
查看答案和解析>>
科目:高中化学 来源: 题型:
H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为________。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为________(填化学式)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com