
【题目】下列物质是电解质的是
A. 氯化钠 B. 铜 C. 二氧化碳 D. 氯气
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,能与有机物和无机物进行反应生成多种氯化物。现用下图装置制取氯气并进行一系列的实验探究。

回答下列问题:
(1)装置1是用来制备纯净、干燥的氯气:
①装置A中圆底烧瓶内发生反应的离子方程式是______________________,反应中被氧化的HCl与消耗的HCl物质的量之比为________________。
②装置B内试剂为_____________,装置C的作用是_____________。
(2)①若将装置1与装置2连接制备少量氯化铁固体(氯化铁易吸水,在300℃时升华),则:D中发生反应的化学方程式为_______________________________。
②若在D装置的硬质玻璃管内装入石英沙和碳粉,则发生如下反应:SiO2+2C+2Cl2![]() SiCl4+2CO。当反应消耗6g碳时,反应转移的电子数为__________,F装置之后还应添加一个装置用来_________。
SiCl4+2CO。当反应消耗6g碳时,反应转移的电子数为__________,F装置之后还应添加一个装置用来_________。
(3)将装置1与装置3连接来探究氯气是否具有漂白性。
①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_____________________。
②为防止氯气尾气污染空气,根据氯水显酸性的性质,可用氢氧化钠溶液吸收多余的氯气,原理是(用离子方程式表示)______________________________。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是_____________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是______________(用字母代号填)。
A.O2 B.H2 C.CO2 D.HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 3A(g)+2B(g) ![]() C(s)+4D(g) △H <0。 图中a、b表示在一定条件下,A的体积分数随时间t的变化。若使曲线b变为曲线a,可采取的措施是
C(s)+4D(g) △H <0。 图中a、b表示在一定条件下,A的体积分数随时间t的变化。若使曲线b变为曲线a,可采取的措施是

A. 增大A的浓度 B. 升高温度 C. 加催化剂 D. 缩小容器体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将a L NH3通入某恒压的密闭容器中,在一定条件下让其分解,达到平衡后气体体积增大到b L(气体体积在相同条件下测定)。下列说法中正确的是
A. 平衡后氨气的分解率为![]() ×100% B. 平衡混合气体中H2的体积分数为
×100% B. 平衡混合气体中H2的体积分数为![]() ×100%
×100%
C. 反应前后气体的密度比为a/b D. 平衡后气体的平均摩尔质量为17a/b g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关“未来金属”钛的信息有:①硬度大②熔点高③常温下耐酸碱、耐腐蚀,由钛铁矿钛的一种工业流程为:

(1)钛铁矿的主要成分是FeTiO3(钛酸亚铁),其中钛的化合价___价,反应①化学方程式为___。
(2)反应②的化学方程式为TiO2+C+Cl![]() TiCl4+CO(未配平),该反应中每消耗12gC,理论上可制备TiCl4___g。
TiCl4+CO(未配平),该反应中每消耗12gC,理论上可制备TiCl4___g。
(3)TiCl4在高温下与足量Mg反应生成金属Ti,反应③化学方程式___,该反应属于___(填基本反应类型)
(4)上述冶炼方法得到的金属钛中会混有少量金属单质是___(填名称),由前面提供的信息可知,除去它的试剂可以是以下剂中的___(填序号)
A HCl BNaOH CNaCl DH2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取镁可按如下步骤进行:①把贝壳(主要成分是碳酸钙)煅烧成生石灰;②在引有海水的渠中加入生石灰,经过沉降,然后过滤得沉淀物;③将沉淀物与稀盐酸反应,然后结晶、过滤、干燥;④电解获得产物。根据上述提取镁的全过程,没有涉及的反应类型是( )
A.分解反应B.化合反应
C.置换反应D.复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁与稀硫酸反应的离子方程式书写正确的是
A. 2Fe + 6H+ = 2Fe3+ + 3H2↑
B. Fe + 2H+ = Fe2+ + H2↑
C. Fe + 2H+ + SO42- = FeSO4↓+ H2↑
D. 2Fe + 6H+ + 3SO42- = Fe2(SO4)3↓+ 3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是主要的温室气体,也是一种工业原料。回收利用CO2有利于缓解温室效应带来的环境问题。
(1)我国科学家通过采用一种新型复合催化剂,成功实现了CO2直接加氢制取高辛烷值汽油。
已知:2H2 (g)+O2 (g) =2H2O(l) ΔH = -571.6 kJ/mol
2C8H18(l)+25O2(g) =16CO2(g)+18H2O(l) ΔH = -11036 kJ/mol
25℃、101kPa条件下,CO2与H2反应生成辛烷(以C8H18表示)和液态水的热化学方程式是_________。
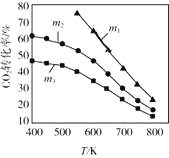
(2)CO2催化加氢合成乙醇的反应原理是:2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol图是起始投料不同时,CO2的平衡转化率随温度的变化关系,m为起始时的投料比,即m=
C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol图是起始投料不同时,CO2的平衡转化率随温度的变化关系,m为起始时的投料比,即m=![]() 。m1、m2、m3投料比从大到小的顺序为_________,理由是_________。
。m1、m2、m3投料比从大到小的顺序为_________,理由是_________。
(3)在Cu/ZnO催化剂存在下,将CO2与H2混合可合成甲醇,同时发生以下两个平行反应:
反应Ⅰ CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH1=-53.7 kJ/mol
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ/mol
反应Ⅱ CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
控制一定的CO2和H2初始投料比,在相同压强下,经过相同反应时间测得如下实验数据(其中“甲醇选择性”是指转化的CO2中生成甲醇的百分比):
实验序号 | T/K | 催化剂 | CO2转化率/% | 甲醇选择性/% |
实验1 | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
实验2 | 543 | Cu/ZnO纳米片 | 10.9 | 72.7 |
实验3 | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
实验4 | 553 | Cu/ZnO纳米片 | 12.0 | 71.6 |
①对比实验1和实验3可发现:同样催化剂条件下,温度升高,CO2转化率升高, 而甲醇的选择性却降低,请解释甲醇选择性降低的可能原因_______________;
②对比实验1和实验 2可发现:在同样温度下,采用Cu/ZnO纳米片使CO2转化率降低, 而甲醇的选择性却提高,请解释甲醇的选择性提高的可能原因____________。
③有利于提高CO2转化为CH3OH平衡转化率的措施有_______。
a.使用Cu/ZnO纳米棒做催化剂
b.使用Cu/ZnO纳米片做催化剂
c.降低反应温度
d.投料比不变,增加反应物的浓度
e.增大![]() 的初始投料比
的初始投料比
(4)以纳米二氧化钛膜为工作电极,稀硫酸为电解质溶液,在一定条件下通入CO2,电解,在阴极可制得低密度聚乙烯![]() (简称LDPE)。
(简称LDPE)。
①电解时,阴极的电极反应式是_____________。
②工业上生产1.4×104 kg 的LDPE,理论上需要标准状况下______L 的CO2。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com