
【题目】亚硝酸钠(NaNO2)是一种常用的发色剂和防腐剂,某学习小组利用如图装置(夹持装置略去)制取亚硝酸钠,已知:2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3;NO能被酸性高锰酸钾氧化为NO3-。下列说法正确的是( )

A.可将B中的药品换为浓硫酸
B.实验开始前通一段时间CO2,可制得比较纯净的NaNO2
C.开始滴加稀硝酸时,A中会有少量红棕色气体
D.装置D中溶液完全褪色后再停止滴加稀硝酸
【答案】C
【解析】
A.装置B中无水CaCl2作干燥剂,干燥NO气体,由于装置为U型管,若换为浓硫酸,气体不能通过,因此不能将B中的药品换为浓硫酸,A错误;
B.实验开始前通一段时间CO2,可排出装置中的空气,避免NO氧化产生NO2气体,不能发生2NO2+Na2O2=2NaNO3,但CO2会发生反应:2CO2+2Na2O2=2Na2CO3+O2,因此也不能制得比较纯净的NaNO2,B错误;
C.开始滴加稀硝酸时,A中Cu与稀硝酸反应产生NO气体,NO与装置中的O2反应产生NO2,因此会有少量红棕色气体,C正确;
D.在装置D中,NO会被酸性KMnO4溶液氧化使溶液褪色,因此当D中溶液紫红色变浅,就证明了NO可以被氧化,此时就可以停止滴加稀硝酸,D错误;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】298K时,二元弱酸H2X溶液中含X微粒的分布分数如图所示。下列叙述正确的是
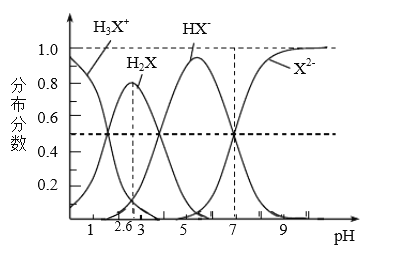
A. 溶液呈中性时: c(Na+)=2c(X2-)
B. Ka2(H2X)为10-7
C. NaHX溶液c( H+)< c(OH-)
D. 溶液pH由1开至2.6时主要存在的反应是: H2X +OH-=HX-+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白皮杉醇具有抗炎、抗菌、抗氧化、抗白血病、提高免疫调节功能等功效,其人工合成过程涉及了如下转化:
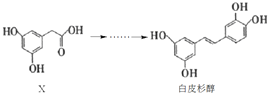
下列说法正确的是
A.X的分子式为C8H10O4
B.化合物X、白皮杉醇均可与Na2CO3溶液反应并放出气体
C.白皮杉醇与浓溴水反应时,最多可消耗6molBr2
D.在一定条件下,白皮杉醇可发生加成、取代、氧化和聚合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃分子的球棍模型(如图),据此回答下列问题:

(1)等质量的上述烃燃烧耗氧量最高的是(填对应字母)__;
(2)属于同系物的是(填对应字母)___;
(3)所有原子都在同一平面上的是(填对应字母)___;
(4)一卤代物总类最多的是(填对应字母)___;
(5)实验室制D的化学方程式___;
(6)写出G合成烈性炸药(TNT)的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式及其叙述正确的是
A.氢气的燃烧热为285.8kJ·mol-1,则水分解的热化学方程式为:2H2O(l)=2H2(g)+O2(g);△H=+571.6kJ·mol-1
B.已知2C(石墨,s)+O2(g)=2CO(g);△H=-221kJ·mol-1,则石墨的燃烧热为110.5 kJ·mol-1
C.已知N2(g)+3H2(g)![]() 2NH3(g) ;△H=-92.4kJ·mol-1,则在一定条件下将1molN2和3molH2置于一密闭容器中充分反应后,放出92.4kJ的热量
2NH3(g) ;△H=-92.4kJ·mol-1,则在一定条件下将1molN2和3molH2置于一密闭容器中充分反应后,放出92.4kJ的热量
D.H+(aq)+OH-(aq)=H2O(l);△H=—57.3kJ/mol,含1molNaOH水溶液与含0.5mol H2SO4的浓硫酸混合后放热57.3kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H3PO4是三元酸,如图是在常温下溶液中含磷微粒的物质的量分数(δ)随pH变化示意图。下列说法不正确的是( )

A.磷酸的第二级电离平衡常数约为10-7.2
B.在NaH2PO4溶液中:c(HPO42-)>c(H3PO4-)
C.在磷酸中滴加NaOH溶液至pH=7,c(Na+)=2c(HPO42)+c(H2PO4)
D.Na3PO4溶液中:c(Na+)=3c(PO43-)+3c(HPO42-)+3c(H2PO4-)+3c(H3PO4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+O3(g)=IO-(aq)+O2(g) △H1
②IO-(aq)+H+(aq)![]() HOI(aq) △H2
HOI(aq) △H2
③HOI(aq)+I-(aq)+H+(aq)![]() I2(aq)+H2O(l) △H3
I2(aq)+H2O(l) △H3
总反应的热化学方程式为___。
(2)AgCl和水的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:写出白色固体转化成黑色固体的化学方程式:___。
(3)向Na2CO3溶液中滴加酚酞呈红色的原因是___(用离子方程式表示);溶液中各离子浓度由大到小的顺序___;向此溶液中加入AlCl3溶液,观察到的现象是__,反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸是重要的化学试剂和工业原料。请回答下列问题:
(1)已知:25℃时,磷酸和氢氟酸的电离常数如下表所示。
物质 | H3PO4 | HF |
电离常数 | Ka1=7.1×10-3;Ka2=6.3×10-8;Ka3=4.2×10-13 | Ka=6.6×10-4 |
向NaF溶液中滴加少量H3PO4溶液,反应的离子方程式为___。
(2)已知:Ⅰ.CaO(s)+H2SO4(l)CaSO4(s)+H2O(l) ΔH=-271kJmol-1
Ⅱ.5CaO(s)+3H3PO4(l)+HF(g)Ca5(PO4)3F(s)+5H2O(l) ΔH=-937kJmol-1
则:①工业上用Ca5(PO4)3F和硫酸反应制备磷酸的热化学方程式为___。
②一定条件下,在密闭容器中只发生反应Ⅱ,达到平衡后缩小容器容积,HF的平衡转化率___(填“增大”“减小”或“不变”,下同);HF的平衡浓度___。
(3)工业上用磷尾矿制备Ca5(PO4)3F时生成的副产物CO可用于制备H2,原理为CO(g)+H2O(g)CO2(g)+H2(g) ΔH。
①一定温度下,向10L密闭容器中充入0.5molCO和1molH2O(g),2min达到平衡时,测得0~2min内用CO2表示的反应速率v(CO2)=0.02molL-1min-1。则CO的平衡转化率α=___;该反应的平衡常数K=___。
②在压强不变的密闭容器中发生上述反应,设起始的(![]() )=y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的ΔH___0(填“>”“<”或“=”,下同)。a___1,理由为___。
)=y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的ΔH___0(填“>”“<”或“=”,下同)。a___1,理由为___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() ,以下是用苯作原料制备一系列化合物的转化关系图:
,以下是用苯作原料制备一系列化合物的转化关系图:
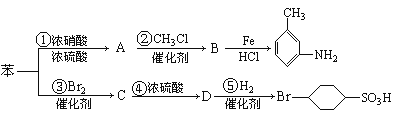
(1)苯转化为A的化学方程式是______________________________________________。
(2)B的结构简式为_______________。
(3)有机物C的所有原子______(填“是”或“不是”)在同一平面上。
(4)D分子苯环上的一氯代物有_________种。
(5)在上述反应①②③④⑤中,属于取代反应的是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com