
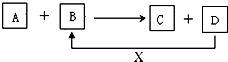
 A、B、C、D、X均为中学化学常见的物质.它们之间存在如图所示转化关系(图中反应条件略去)
A、B、C、D、X均为中学化学常见的物质.它们之间存在如图所示转化关系(图中反应条件略去)

科目:高中化学 来源: 题型:
| A、丙烷的二溴取代产物比其六溴取代产物的种类少 |
| B、除去乙烯中的少量的二氧化硫方法是将混合气体通过酸性高锰酸钾溶液 |
C、由CH2═CCNCH3合成的聚合物为 |
| D、正丁烷和异丁烷的熔、沸点不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、人造纤维、合成橡胶和光导纤维都属于有机高分子化合物 |
| B、使用生物酶降解生活废水中的有机物,可防止水体的富营养化 |
| C、上海世博会很多展馆采用光电转化装置,体现当今“低碳”经济的理念 |
| D、利用二氧化碳等原料合成聚碳酸酯类可降解塑料,有利于减少白色污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖.
我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖.查看答案和解析>>
科目:高中化学 来源: 题型:
| 方法Ⅰ | 用氨水将SO2转化(NH4)2SO3,再氧化成(NH4)2SO4 |
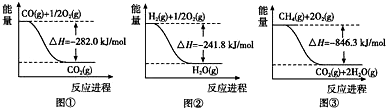
| 方法Ⅱ | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
| 方法Ⅲ | 用Na2SO3溶液吸收SO2,再经电解转化为H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol?L-1 | 0.5 | 2 | 2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、③④⑤ | C、③⑤ | D、③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com