
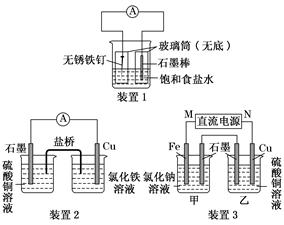
 2Cu+O2↑+4H+ ③224
2Cu+O2↑+4H+ ③224 2Cu+O2↑+4H+;
2Cu+O2↑+4H+;

科目:高中化学 来源:不详 题型:单选题
| A.通过煤的干馏可获得苯、甲苯等芳香烃 |
| B.在海轮外壳装上锌块,可减缓船体的腐蚀速率 |
| C.电渗析法、离子交换法中,只有后者可以应用于海水的淡化 |
| D.我国城市推广使用清洁燃料是压缩天然气类和液化石油气类 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
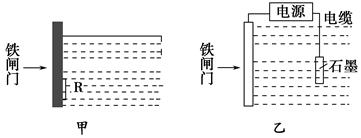
| A.铜 | B.钠 | C.锌 | D.石墨 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
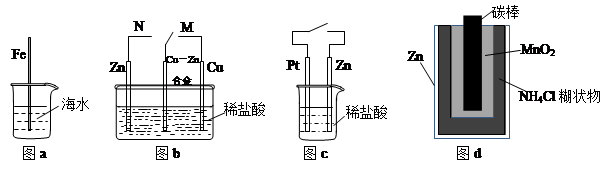
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.纯银器表面在空气中会因化学腐蚀渐渐变暗 |
| B.地下输油钢管与外加直流电源的正极相连可保护其不受腐蚀 |
| C.海轮外壳连接锌块是采用牺牲阴极的阳极保护法保护外壳不受腐蚀 |
| D.当镀锡铁制品的镀层破损时,锡镀层仍能对铁制品起保护作用 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
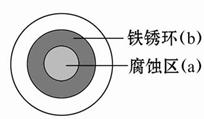
| A.液滴中的Cl-由a区向b区迁移 |
| B.液滴边缘是正极区,发生的电极反应为O2+2H2O+4e-=4OH- |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为Cu-2e-=Cu2+ |
查看答案和解析>>
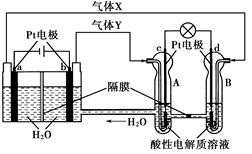
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
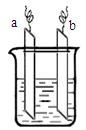
| A.a、b可能是同种电极材料 |
| B.该装置一定是电解池 |
| C.装置中电解质溶液一定含有Ag+ |
| D.装置中发生的反应方程式一定是Fe+2Ag+==Fe2++2Ag |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2H++2e-=H2↑ | B.2H2O+O2+4e-=4OH- |
| C.Fe-2e-=Fe2+ | D.4OH--4e-=O2↑+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com