
��16�֣�ijҩѧ��־������һ�־������Կ������Ե�ҩ���ṹ��ͼ��ʾ��J����ͬ���칹�壬J�ĺϳ�·�����£����ֲ�������ȥ����
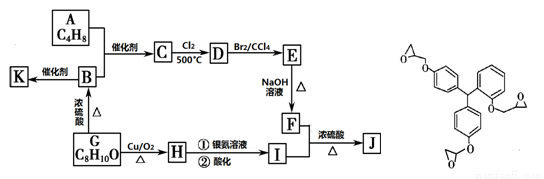
��֪���� CH2=CHR1 + CH2=CHR2  CH2=CH2 + R1CH=CHR2
CH2=CH2 + R1CH=CHR2
�� R��CH2��CH=CH2 + Cl2 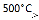 R��CHCl��CH=CH2 + HCl
R��CHCl��CH=CH2 + HCl
�� �˴Ź�������ͼ��ʾA�����в�ͬ������ԭ�Ӹ�����Ϊ3 ��1��F����֬ˮ��IJ���֮һ������ˮ������������ܣ�K��һ�ָ߷��ӻ����
��ش��������⣺
��1����ҩ����ܾ��е������� ������ĸ��ţ���
a��������ˮ b���ܷ����ӳɷ�Ӧ c���ܷ���ˮ�ⷴӦ d���ܷ���ȡ����Ӧ
��2��H�����к��й����ŵ������� ��G�Ľṹ��ʽΪ ��
��3������ϵͳ��������A�������� ��
��4��C��D�ķ�Ӧ����Ϊ ��
��5��д�����з�Ӧ�Ļ�ѧ����ʽ��
B��K ��F��I��J ��
��6��д��ͬʱ��������������I������ͬ���칹��Ľṹ��ʽ ��
�ٷ����к��б����ṹ�����ܷ���������Ӧ���۱����ϵ�һ�ȴ��������֡�
��16�֣���1��bd��2�֣�
��2��ȩ�� ��1�֣� 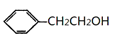 ��2�֣�
��2�֣�
��3��2-��ϩ��2�֣�
��4��ȡ����Ӧ��1�֣�
��5��
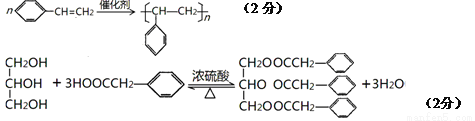
��6��
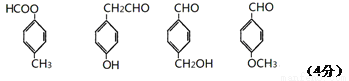
��������
�����������1����ҩ���к��б��������Կ��Է����ӳɷ�Ӧ��ȡ����Ӧ�������ܷ���ˮ�ⷴӦ���Ҳ�����ˮ�������Բ�����ˮ����˴�ѡbd��
��2������H�����ķ�Ӧ���������ж�H�к���ȩ������G�к���-CH2OH�ṹ���˴Ź�������ͼ��ʾA�����в�ͬ������ԭ�Ӹ�����Ϊ3 ��1����A��2-��ϩ��KΪ�߷��ӻ����������Ŀ��֪��Ϣ������B�к�̼̼˫��������G�ɷ�����ȥ��Ӧ������ж�G�Ľṹ��ʽΪ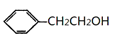 ��
��
��3���ɣ�2���ɵ�A��������2-��ϩ��
��4��������֪���ж�C��D�ķ�Ӧ����ȡ����Ӧ��
��5��BΪ����ϩ�������Ӿ۷�Ӧ����K����ѧ����ʽΪ
 ��F����֬ˮ��IJ���֮һ��������ͼ���ж�F���ڴ��࣬����F�Ǹ��ͣ�IΪ�����ᣬ���߷���������Ӧ����J����ѧ����ʽΪ
��F����֬ˮ��IJ���֮һ��������ͼ���ж�F���ڴ��࣬����F�Ǹ��ͣ�IΪ�����ᣬ���߷���������Ӧ����J����ѧ����ʽΪ 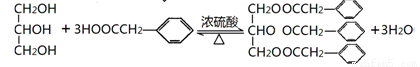 ��
��
��6���ܷ���������Ӧ��˵�������д���-CHO�������ϵ�һ�ȴ��������֣�����I�Ľṹ��ʽ�ж���ͬ���칹��Ľṹ�д��ڶ�λ��2����ͬȡ���������Է���������I��ͬ���칹����4�֣��ֱ���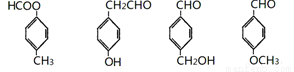
���㣺�����л��ƶϣ��ṹ��ʽ����ѧ����ʽ����д�������������жϣ��л����������ͬ���칹����жϼ���д



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014��������ѧ�����п��Ը߶���ѧ�Ծ��������棩 ���ͣ�ѡ����
������ѧ�ҽ�����Ԫ��Ǧ��봵�ԭ�Ӻ˶�ײ�������һ��������118��������Ϊ175�ij���
Ԫ�أ���Ԫ��ԭ�Ӻ�������������������֮���ǣ� ��
A��57 B��47 C��61 D��293
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������У���˸����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
һ�������£�������Ӧ����M(s)+N(g)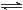 R(g) ��H = ��Q1 kJ��mol��1����2R (g)+N(g)
R(g) ��H = ��Q1 kJ��mol��1����2R (g)+N(g)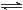 2T (g) ��H = ��Q2 kJ��mol��1�� Q1��Q2 ��Q3��Ϊ��ֵ������˵����ȷ����
2T (g) ��H = ��Q2 kJ��mol��1�� Q1��Q2 ��Q3��Ϊ��ֵ������˵����ȷ����
A��1 mol R(g)�������ܺʹ���1 mol M(s)��1 mol N(g) �������ܺ�
B����2 mol R (g)��1 mol N(g)�ڸ������³�ַ�Ӧ,�ų�����Q2 kJ
C����1 mol M(s)��ȫת��ΪT (g)ʱ(�ٶ���������ʧ)���ų�����Q1+ kJ
kJ
D��M(g)+N(g)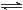 R(g) ��H=��Q3 kJ��mol��1 , ��Q3 ��Q1
R(g) ��H=��Q3 kJ��mol��1 , ��Q3 ��Q1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������У����5�µ���������Կ������ۻ�ѧ�Ծ��������棩 ���ͣ������
��14�֣��й����������վ������ʾ��������(PM2.5��)Ϊ������������Ӱ�������������������Ⱦ�����ҪΪȼú��������β���ȡ���ˣ���PM2.5��SO2��NOx�Ƚ����о�������Ҫ���塣��ش��������⣺
��1����PM2.5����������ˮ�����Ƴɴ�������������ø���������ˮ���������ӵĻ�ѧ��ּ���ƽ��Ũ�����±���
���� | K+ | Na+ | NH | SO | NO | Cl�� |
Ũ��/mol?L��1 | 4��10��6 | 6��10��6 | 2��10��5 | 4��10��5 | 3��10��5 | 2��10��5 |
���ݱ������ݼ���PM2.5����������pH ���� ����
��2�� NOx������β������Ҫ��Ⱦ��֮һ����������������ʱ������N2��O2��Ӧ���������仯ʾ��ͼ���£�

�� N2(g)��O2(g) 2NO(g)��H�� ��
2NO(g)��H�� ��
�ڵ�β���п�������ʱ��NOx�ڴ�ת�����б���ԭ��N2�ų���д��NO��CO��ԭ�Ļ�ѧ����ʽ ��
�� �������Ͳ���ȫȼ��ʱ������CO���������밴���з�Ӧ��ȥCO��
2CO(g)��2C(s)��O2(g),��֪�÷�Ӧ�ġ�H��0���������ܷ�ʵ�֣� ��
��3����ѭ�����ղ���������SO2���ͻ�����Ⱦ��ͬʱ�����Ƶ������������������£�

�� �����ӷ���ʽ��ʾ��Ӧ���з����ķ�Ӧ�� ����
�� �û�ѧƽ���ƶ���ԭ����������HI�ֽⷴӦ��ʹ��Ĥ��Ӧ�������H2��Ŀ���� ��
�� ������H2���ϡ������Ͻ���Ϊ��ظ�������(��MH��ʾ����NiO(OH)��Ϊ����������ϣ�KOH��Һ��Ϊ�������Һ�����Ƶø��������������������ء���س�ŵ�ʱ���ܷ�ӦΪ��Ni(OH)2��M  NiO(OH)��MH����طŵ�ʱ�������缫��ӦʽΪ�� ���� ������ʱ��ȫ��ת��ΪNiO(OH)����������磬����һ���缫����O2��O2��ɢ����һ���缫�����缫��Ӧ�����ģ��Ӷ�������������������ر�ը��
NiO(OH)��MH����طŵ�ʱ�������缫��ӦʽΪ�� ���� ������ʱ��ȫ��ת��ΪNiO(OH)����������磬����һ���缫����O2��O2��ɢ����һ���缫�����缫��Ӧ�����ģ��Ӷ�������������������ر�ը��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������У����5�µ���������Կ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
4�ֶ�����Ԫ��W��X��Y��Z��ԭ����������������ԭ�ӵ�����������֮��Ϊ19��W��XԪ��ԭ����������֮��Ϊ1��2��X2+��Z�����ӵĵ�����֮��Ϊ8������˵������ȷ����
A����W���ڵ�ͬ����Ԫ�ؿ��Ƴ���Ҫ�İ뵼�����
B��Ԫ��ԭ�Ӱ뾶�Ӵ�С��˳����X��Y��Z
C��WZ4������W��Zԭ��ͨ�����ۼ�������������ﵽ8���ӽṹ
D��W��Y��ZԪ�ض�Ӧ���⻯���ȶ�����ǿ����H2Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������������������ѧ�ڵڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A�����۵�Ĺ�������������Ӿ��壬��һ��Ϊԭ�Ӿ���
B�������������ǿ������������ԣ�����֪�����ԣ�Cl2>S
C��������Ԫ����ɵĹ��ۻ���������У�ֻ���ܴ��ڼ��Լ�
D����X+ ��Y2���ĺ�����Ӳ�ṹ��ͬ����ԭ��������X>Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������ѧ�ڸ����ڶ�����ϲ��������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
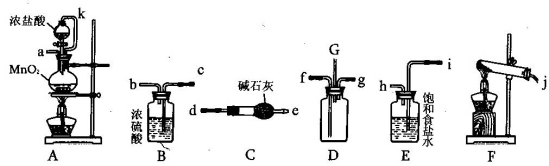
(15��)ij��ѧ��ȤС���������¸�װ�����ӳ�һ����װ�ã�̽�������백��֮��ķ�Ӧ������DΪ��������������봿�����ﰱ����Ӧ��װ�ã�
��ش��������⣺
(1)���Ӻ�װ�ú�����е�һ��ʵ�������__________________
(2)װ��E��������____________����k��������________________________
(3)��װ��D��G���ݳ���β���п��ܺ��л���ɫ���ж����壬����������__________________
(4)װ��F���Թ��ڷ�����Ӧ�Ļ�ѧ����ʽ____________________________________
(5)����Dװ�õ�����������߽ϳ����ұ߽϶̣�Ŀ����______________________________
(6)����װ�ô������ҵ�����˳����(j)��( ) ( )��(f) (g)��( ) ( )��( ) ( )��(a)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������������������ǰģ�����ۻ�ѧ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ����
A��lmol Cl2ͨ�뺬��2mol FeI2����Һ�У�2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
B������ʯ��ˮ������С�մ���Һ��ϣ�Ca2++OH-+ HCO3-=CaCO3��+H2O
C��AlCl3��Һ�м��������ˮ��Al3++4 OH-= AlO-2+2H2O
D����������Һ�м������������[Ag(NH3)2]++OH-+3H+= Ag++2NH4++ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и���˫�����Ի�ѧ�Ծ��������棩 ���ͣ������
��15�֣���1��25��ʱ��0��1 mol��L��1��HA��Һ��c(H+)/c(OH-)��1010����ش��������⣺
��HA��________(�ǿ����ʡ���������ʡ�)��
���ڼ�ˮϡ��HA��Һ�Ĺ����У�����ˮ�������Ӷ���С����________(����ĸ)��
A��c(H+)/c(HA)�� B��c(HA)/(A-) C��c(H��)��c(OH��)�ij˻� ��D��c(OH��)
����M��Һ��������HA��ҺV1 mL��pH = 12��NaOH��ҺV2 mL��ϳ�ַ�Ӧ���ã�������˵������ȷ����
A������ҺM�����ԣ�����ҺM��c(H+) + c(OH-) = 2��0��10-7 mol��L-1
B����V1 =V2 ������ҺM��pHһ������7
C������ҺM�����ԣ�V1һ������V2
D������ҺM�ʼ��ԣ�V1һ��С��V2
��2������֪��25�棬AgCl��Ksp = 1��8��10-10���ֽ�����AgCl�ֱ���룺��100 mL ����ˮ�У���100 mL 0��2mol��L-1 AgNO3��Һ�У���100 mL 0��1mol��L-1 AlCl3��Һ�У���100 mL 0��1mol��L-1�����У���ֽ������ͬ�¶���c(Ag+)�ɴ�С��˳���� ����������ӣ�
��3����1mol SO2(g)����Ϊ1mol SO3(g)�Ħ�H ����99kJ��mol��1���������ȼ����Ϊ296kJ��mol��1������S(s)����3 mol SO3(g)�Ħ�H =
��4������2NO2(g) N2O4(g) ��H < 0��Ӧ�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ��������˵����ȷ���� ��
N2O4(g) ��H < 0��Ӧ�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ��������˵����ȷ���� ��

�٣�A��C����ķ�Ӧ���ʣ�A>C
�ڣ�A��C�����������ɫ��A�Cdz
�ۣ�B��C����������ƽ������������B<C
�ܣ���״̬B��״̬A�������ü��ȷ���
��5����ͼ�����ü���ȼ�ϵ�ص��50 mL 2 mol��L-1���Ȼ�ͭ��Һ��װ��ʾ��ͼ��
��ش�
�� ����ȼ�ϵ�صĸ�����Ӧʽ�� ��
�� ����·����0��2 mol����ͨ��ʱ����������____g��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com