

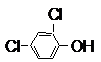 .
. 分析 利用甲酯除草醚结构简式: 和生成D的反应可以确定C为
和生成D的反应可以确定C为
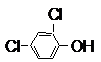
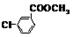 ;由B结合题中信息:酰氯(RCOCl或
;由B结合题中信息:酰氯(RCOCl或)中的氯原子很活泼,易水解或醇解,可推知A的结构简式
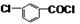 ,以此来解答.
,以此来解答.
解答 解:利用甲酯除草醚结构简式: 和生成D的反应可以确定C为
和生成D的反应可以确定C为
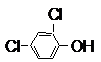
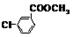 ;由B结合题中信息:酰氯(RCOCl或
;由B结合题中信息:酰氯(RCOCl或)中的氯原子很活泼,易水解或醇解,可推知A的结构简式
 ,
,
(1)甲酯除草醚结构简式为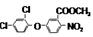 ,存在官能团为氯原子、硝基、酯基、醚键,故答案为:氯原子、硝基;
,存在官能团为氯原子、硝基、酯基、醚键,故答案为:氯原子、硝基;
(2)由上述分析可知,D的结构简式是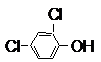
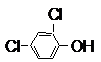
点评 本题考查有机物的合成,为高频考点,把握合成流程中官能团的变化、有机反应及合成信息等为解答的关键,侧重分析与推断能力的考查,注意有机物的结构与性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将0.1mol•L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液 | 先有白色沉淀生成后变为蓝色沉淀 | Cu(OH)2的Ksp比Mg(OH)2的小 |
| B | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+,无K+ |
| C | 向盛Na2SiO3 溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2min后,试管里出现凝胶 | 非金属性:Cl>Si |
| D | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状碳 | 浓硫酸具有吸水性和强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
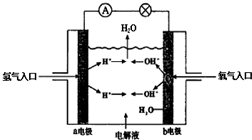
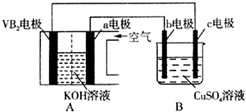 碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5.用该电池电解200mL硫酸铜溶液,实验装置如图所示(b、c均为惰性电极),当外电路中通过0.04mol电子时,B装置两极共收集到0.448L气体(标准状况).下列说法正确的是( )
碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5.用该电池电解200mL硫酸铜溶液,实验装置如图所示(b、c均为惰性电极),当外电路中通过0.04mol电子时,B装置两极共收集到0.448L气体(标准状况).下列说法正确的是( )| A. | 电解过程中,b电极表面先有红色物质析出,然后有气泡产生 | |
| B. | VB2为负极,电极反应为:2VB2+11H2O-22e-=V2O5+2B2O3+22H+ | |
| C. | 电池内部OH-移向a电极,溶液pH减小 | |
| D. | 忽略溶液体积变化,电解后B装置中溶液的pH为1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入碳酸锰的目的是除去Fe3+ | |
| B. | 常温下pH=4时,Fe3+已除尽 | |
| C. | Cu2+(aq)+MnS(s)=CuS(s)+Mn2+(aq)的K=2.73×10-23 | |
| D. | Mn2(OH)2CO3、Mn(OH)2都可以替代MnCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 碳原子数(n) | 6 | 8 | 10 | 12 | … |
| 结构简式 | 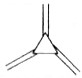 | 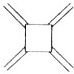 | 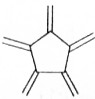 | 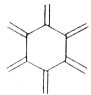 | … |
| A. | 轴烯的通式可表示为CnHn | |
| B. | n=100的轴烯分子中含有50个碳碳双键 | |
| C. | n=6的轴烯分子的同分异构体中含有两个碳碳三键的结构有6种 | |
| D. | n=8的轴烯分子的同分异构体可能属于芳香烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | RO | B. | R2Om | C. | R2Om-n | D. | R2O2m-n |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
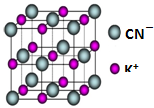 目前工业上制备丙烯腈(CH2=CHC≡N)有乙炔法、丙烯氨氧化法等.
目前工业上制备丙烯腈(CH2=CHC≡N)有乙炔法、丙烯氨氧化法等.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com