
| A. | 2H2(g)+O2(g)═2H2O(l) | |
| B. | 4Al(s)+3O2(g)═2Al2O3(s) | |
| C. | 2Na(s)+2H2O(l)═2Na+(aq)+2OH- (aq)+H2(g) | |
| D. | 2H+(aq)+SO42-(aq)+Ba2+(aq)+2OH- (aq)═BaSO4(s)+2H2O(l) |
分析 金属与酸反应、燃烧反应、中和反应均为放热反应,结合化学计量数可知,气体的体积增大或溶液中生成更多的离子,则混乱度增大,以此来解答.
解答 解:A.2H2(g)+O2(g)═2H2O(l)中混乱度减小,故A不选;
B.4Al(s)+3O2(g)═2Al2O3(s)中混乱度减小,故B不选;
C.2Na(s)+2H2O(l)═2Na+(aq)+2OH- (aq)+H2(g)为放热反应,且混乱度增加,故C选;
D.2H+(aq)+SO42-(aq)+Ba2+(aq)+2OH- (aq)═BaSO4(s)+2H2O(l)中混乱度减小,故D不选;
故选C.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、混乱度判断为解答的关键,侧重分析与应用能力的考查,注意溶液中离子数目增多时混乱度增大,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 元素X、W的简单阴离子具有相同的电子层结构 | |
| B. | 原子半径:r(Y)<r(X)<r(W)<r(Z) | |
| C. | W的简单气态氢化物的热稳定性比Y的强 | |
| D. | 由X、Z两种元素组成的化合物是离子化合物,只含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
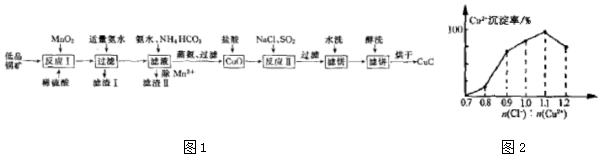
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 有机物 | 同分异构体数目 |
| A | 分子式为C5H10O2的酯 | 10 |
| B | 分子式为C5H10,能使溴的四氯化碳溶液褪色 | 5 |
| C | 分子式为C4H10O,能与Na反应生成氢气 | 4 |
| D | 分子式为C8H10的芳香烃 | 4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3易液化,液氨常用作制冷剂 | |
| B. | 与金属反应时,稀HNO3可能被还原为更低价态,则HNO3氧化性强于浓HNO3 | |
| C. | 氨盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉通风处 | |
| D. | 由NH3制碳酸氢铵和硫酸铵不是氮的固定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56gCO和32gO2所具有的总能量大于88gCO2所具有的总能量 | |
| B. | △H1=△H3>△H2 | |
| C. | △H1<△H3 | |
| D. | 28gCO的能量比44gCO2的能量高 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 雷雨时空气中的 N2转化为NO | B. | 硝酸工厂用NH3氧化制NO | ||
| C. | N2与H2在一定条件下反应生成NH3 | D. | 由NH3制碳酸氢铵和硫酸铵 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com