
| A. | 用稀氨水鉴别Al3+、Mg2+和Ag+ | |
| B. | 用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷 | |
| C. | 用酸性KMnO4溶液鉴别CH3CH═CHCH2OH和CH3CH2CH2CHO | |
| D. | 用Ba(NO3)2溶液鉴别Cl-、SO42-和CO32- |
分析 A.稀氨水和Al3+、Mg2+都反应生成白色沉淀,稀氨水先和Ag+反应生成AgOH沉淀,后AgOH和氨水反应生成银氨络合物;
B.1-溴丙烷和2-溴丙烷中分别有3种、2种位置的H;
C.碳碳双键和醛基都能被酸性高锰酸钾氧化而使酸性高锰酸钾溶液褪色;
D.Ba 2+和SO42-、CO32-都反应生成白色沉淀.
解答 解:A.稀氨水先和Ag+反应生成AgOH沉淀,后AgOH和氨水反应生成银氨络合物,看到的现象是先生成沉淀后沉淀溶解;稀氨水和Al3+、Mg2+都反应生成白色沉淀,现象相同,无法鉴别,故A错误;
B.1-溴丙烷和2-溴丙烷中分别有3种、2种位置的H,则用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷,故B正确;
C.碳碳双键和醛基都能被酸性高锰酸钾氧化而使酸性高锰酸钾溶液褪色,所以不能用酸性高锰酸钾溶液鉴别,可以用银氨溶液鉴别,故C错误;
D.Ba 2+和SO42-、CO32-都反应生成白色沉淀,现象相同无法鉴别,故D错误;
故选B.
点评 本题考查物质检验鉴别实验方案设计,为高频考点,明确物质性质差异性是解本题关键,知道常见有机物官能团及其性质关系,易错选项是C.


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
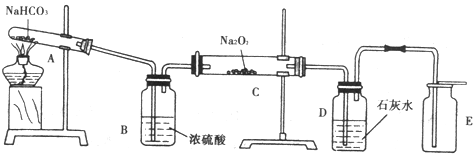
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
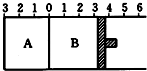 如图所示,温度不变下某容器分隔AB两部分,A容积固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2mol SO3和1molN2,开始时活塞停在3处.在相同条件下发生可逆反应:2SO3(g)?2SO2(g)+O2(g),则下列说法正确的是( )
如图所示,温度不变下某容器分隔AB两部分,A容积固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2mol SO3和1molN2,开始时活塞停在3处.在相同条件下发生可逆反应:2SO3(g)?2SO2(g)+O2(g),则下列说法正确的是( )| A. | A中的压强大于B中的压强 | |
| B. | A中的SO2浓度小于B中SO2浓度 | |
| C. | A中的SO3浓度小于B中SO3浓度 | |
| D. | 将A改为可移动的活塞,达平衡时,A 停在0左侧0.5 处,则B可能停在0右侧3.2处 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
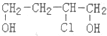 )是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂.
)是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂.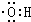 .
.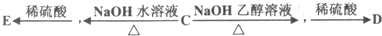
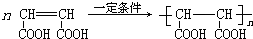 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸与水 | B. | 氯化钠与水 | C. | 熟石灰与水 | D. | 生石灰与水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雾霾--CO | B. | 白色污染--废弃塑料 | ||
| C. | 酸雨--SO2 | D. | 温室效应--CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com