
”¾ĢāÄæ”æ
£Ø1£©Ń”ŌńŅĒĘ÷£®Ķź³É±¾ŹµŃéĖł±ŲŠčµÄŅĒĘ÷ÓŠ£ŗĶŠÅĢĢģĘ½£Ø¾«Č·µ½0.1g£©”¢Ņ©³×”¢ÉÕ±”¢²£Į§°ō”¢________”¢________ŅŌ¼°µČÖŹĮæµÄĮ½Ę¬ĀĖÖ½£®
£Ø2£©¼ĘĖć£®ÅäÖĘøĆČÜŅŗŠčČ”NaCl¾§Ģå_________g£®
£Ø3£©³ĘĮ森¢ŁĢģĘ½µ÷Ę½Ö®ŗó£¬Ó¦½«ĢģĘ½µÄÓĪĀėµ÷ÖĮijøöĪ»ÖĆ£¬ĒėŌŚĶ¼1ÖŠÓĆŅ»øłŹśĻß±ź³öÓĪĀė×ó±ßŌµĖł“¦µÄĪ»ÖĆ£ŗ

¢Ś³ĘĮæ¹ż³ĢÖŠNaCl¾§ĢåÓ¦·ÅÓŚĢģĘ½µÄ________£ØĢī”°×óÅĢ”±»ņ”°ÓŅÅĢ”±£©£®
¢Ū³ĘĮæĶź±Ļ£¬½«Ņ©Ę·µ¹ČėÉÕ±ÖŠ£®
£Ø4£©Čܽā”¢ĄäČ“£¬øĆ²½ŹµŃéÖŠŠčŅŖŹ¹ÓĆ²£Į§°ō£¬ÄæµÄŹĒ__________£®
£Ø5£©×ŖŅĘ”¢Ļ“µÓ£®ŌŚ×ŖŅĘŹ±Ó¦Ź¹ÓĆ________ŅżĮ÷£¬ŠčŅŖĻ“µÓÉÕ±2”«3“ĪŹĒĪŖĮĖ________£®
£Ø6£©¶ØČŻ£¬Ņ”ŌČ£®
£Ø7£©½«ÅäŗƵÄČÜŅŗ¾²ÖĆŅ»¶ĪŹ±¼äŗ󣬵¹ČėÖø¶ØµÄŹŌ¼ĮĘ棬²¢ĢłŗƱźĒ©£¬×¢Ć÷ÅäÖʵď±¼ä”¢________”¢________£®
£Ø8£©ŌŚÅäÖĘ¹ż³ĢÖŠ£¬Ä³Ń§Éś¹Ū²ģ¶ØČŻŹ±ŅŗĆęĒéæöČēĶ¼2ĖłŹ¾£¬ĖłÅäČÜŅŗµÄÅØ¶Č»į________£ØĢī”°Ę«øß”±”¢”°Ę«µĶ”±»ņ”°ĪŽÓ°Ļģ”±£©£®
”¾“š°ø”æ£Ø1£©500mLČŻĮæĘæ½ŗĶ·µĪ¹Ü£Ø2£©14.6
£Ø3£©×óÅĢ£Ø4£©½Į°č£¬¼ÓĖŁNaClČܽā
£Ø5£©²£Į§°ō£¬±£Ö¤ČÜÖŹČ«²æ×ŖŅĘČėČŻĮæĘæÖŠ£Ø7£©ÅضČĆū³ĘĘ«µĶ
”¾½āĪö”æŹŌĢā·ÖĪö£ŗ£Ø1£©ÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗŠčŅŖÓƵ½ĶŠÅĢĢģĘ½£ØĮæĶ²£©”¢ÉÕ±”¢²£Į§°ō”¢ČŻĮæĘ攢½ŗĶ·µĪ¹Ü£¬ČŻĮæĘæµÄ¹ęøńŹĒ100mL”¢250mL”¢500mL”¢1000mL£¬Ņņ“ĖŠčŅŖ500mLČŻĮæĘæŗĶ½ŗĶ·µĪ¹Ü£»
£Ø2£©ŠčŅŖĀČ»ÆÄʵÄÖŹĮæĪŖm£ØNaCl£©£½500”Į10£3”Į0.5”Į58.5g=14.6g£»
£Ø3£©øł¾ŻĶŠÅĢĢģĘ½µÄŹ¹ÓĆ”°×óĪļÓŅĀė”±æÉÖŖNaCl¾§Ģå·ÅŌŚĢģĘ½µÄ×óÅĢ£»
£Ø4£©ČܽāŹ¹ÓĆ²£Į§°ō½ųŠŠ½Į°č£¬¼ÓĖŁĀČ»ÆÄʵÄČܽā£»
£Ø5£©×ŖŅĘŹ±Ó¦Ź¹ÓĆ²£Į§°ōŅżĮ÷£¬·ĄÖ¹ČÜŅŗ½¦µ½ĶāĆę£¬Ōģ³ÉĖłÅäÅØ¶Č²»×¼£¬ŠčŅŖĻ“µÓÉÕ±ŗĶ²£Į§°ō2”«3“Ī£¬ĪŖĮĖ±£Ö¤ČÜÖŹČ«²æ×ŖŅĘČėČŻĮæĘæÖŠ£»
£Ø7£©½«ÅäŗƵÄČÜŅŗ¾²ÖĆŅ»¶ĪŹ±¼äŗ󣬵¹ČėÖø¶ØµÄŹŌ¼ĮĘ棬²¢ĢłŗƱźĒ©£¬×¢Ć÷ÅäÖʵď±¼ä”¢ÅØ¶Č”¢Ćū³Ę£»
£Ø8£©ŃöŹÓ¶ĮŹż£¬ĖłÅäČÜŅŗĢå»żŌö“ó£¬ČÜÖŹµÄĪļÖŹµÄĮæ²»±ä£¬Ņņ“ĖÅØ¶Č½«Ę«µĶ”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖĮĖ³żČ„KClČÜŅŗÖŠÉŁĮæµÄMgCl2”¢MgSO4£¬æÉŃ”ÓĆBa(OH)2”¢HClŗĶK2CO3ČżÖÖŹŌ¼Į£¬°“ĻĀĶ¼²½Öč²Ł×÷£ŗ
![]()
£Ø1£©Š“³öČżÖÖŹŌ¼ĮµÄ»ÆѧŹ½£ŗA_____ ___£¬B_ _______£¬C_ _______”£
£Ø2£©¼Ó¹żĮæAµÄŌŅņŹĒ£ŗ__________________£¬
ÓŠ¹Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ__________________£¬_________________”£
£Ø3£©¼Ó¹żĮæBµÄŌŅņŹĒ£ŗ__________________________£¬
ÓŠ¹Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ_________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×ÓÄÜøśH+“óĮæ¹²“ęµÄŹĒ
A. OH- B. CO32- C. SO32- D. SO42-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ( )
¢Ł±ź×¼×“æöĻĀ£¬ŗ¬NAøöė²Ō×ÓµÄė²ĘųĢå»żŌ¼ĪŖ22.4L ¢Ś34g H2O2ÖŠŗ¬ÓŠµÄŅõĄė×ÓŹżĪŖNA ¢Ū³£ĪĀ³£Ń¹ĻĀ£¬21gŃõĘųŗĶ27g³ōŃõÖŠŗ¬ÓŠµÄŃõŌ×Ó×ÜŹżĪŖ3NA ¢ÜŌŚFe²ĪÓėµÄ·“Ó¦ÖŠ£¬1mol FeŹ§Č„µÄµē×ÓŹżĪŖ3NA ¢Ż±ź×¼×“æöĻĀ£¬11.2LµÄCl2ČÜÓŚĖ®£¬×ŖŅʵĵē×Ó×ÜŹżĪŖ0.5NA ¢ŽŌŚO2²ĪÓėµÄ·“Ó¦ÖŠ£¬1mol O2×÷Ńõ»Æ¼ĮŹ±µĆµ½µÄµē×ÓŹżŅ»¶ØŹĒ4NA ¢ß1L 1mol”¤L©1NH4NO3ČÜŅŗÖŠµŖŌ×ÓŹżŠ”ÓŚ2NA ¢ą±ź×¼×“æöĻĀ£¬22.4L CCl4ÖŠĖłŗ¬ÓŠµÄ·Ö×ÓŹżĪŖNA£®
A£®¢Ł¢Ś¢Ż B£®¢Ł¢Ž¢ą C£®¢Ł¢Ū D£®¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅÖŠĖłÓĆÉŁĮæĀČĘųŹĒÓĆĻĀĮŠ·½·ØÖĘČ”µÄ£¬4HCl£ØÅØ£©£«MnO2![]() Cl2”ü£«MnCl2£«2H2O
Cl2”ü£«MnCl2£«2H2O
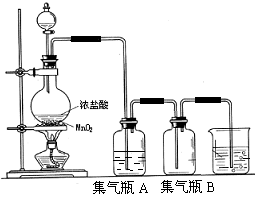
ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĒėÖø³ö ŹĒŃõ»Æ¼Į£¬ _ŹĒ»¹Ō¼Į£¬Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ ”£
£Ø2£©¼ÆĘųĘæAÖŠŹ¢×°µÄŹĒ±„ŗĶŹ³ŃĪĖ®£Ø×¢£ŗĀČĘųŌŚ±„ŗĶŹ³ŃĪĖ®ÖŠČܽā¶ČŗÜŠ”£¬¶ųĀČ»ÆĒāŌŚ±„ŗĶŹ³ŃĪĖ® ÖŠµÄČܽā¶ČŌņŗܓ󣩣¬Ęä×÷ÓĆŹĒ ”£
£Ø3£©ĀČĘųČÜČėĖ®ĻŌĖįŠŌ£¬ĒŅĀČĘųÓŠ¶¾£¬²¢ÓŠ¾ēĮŅµÄ“Ģ¼¤ŠŌ£¬ČōĪüČė“óĮæĀČĘų£¬æÉÖŠ¶¾ĖĄĶö£¬ĖłŅŌĀČĘųĪ²ĘųÖ±½ÓÅÅČė“óĘųÖŠ£¬»įĪŪČ¾»·¾³”£ŹµŃéŹŅÖŠæɲÉÓĆ ČÜŅŗĄ“ĪüŹÕÓŠ¶¾µÄĀČĘų”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬¼×”¢ŅŅĮ½Ęæ°±Ė®µÄÅØ¶Č·Ö±šĪŖ1mol/LŗĶ0.1mol/L£¬Ōņ¼×”¢ŅŅĮ½Ęæ°±Ė®ÖŠc (OH-)Ö®±ČĪŖ( )
A£®“óÓŚ10 B£®Š”ÓŚ10 C£®µČÓŚ10 D£®ĪŽ·ØČ·¶Ø
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ
A. Ķ¬Ņ»ÉśĪļĢå²»Ķ¬×éÖÆĻø°ūÄŚ»ÆѧŌŖĖŲÖÖĄąŗĶŗ¬Įæ“óĢåĻąĶ¬
B. C”¢H”¢O”¢NŹĒ×é³ÉÉśĪļĢåÄŚĆøĖł±ŲŠčµÄŌŖĖŲ
C. µ°°×ÖŹÖŠµÄSŌŖĖŲ“ęŌŚÓŚ°±»łĖįµÄR»łÖŠ
D. Õ¼Ļø°ūµÄĻŹÖŲ×ī¶ąµÄŌŖĖŲŹĒO
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹Ų»Æѧ¼üµÄŠšŹö£¬ÕżČ·µÄŅ»ĻīŹĒ
A£®Ąė×Ó»ÆŗĻĪļÖŠŅ»¶Øŗ¬ÓŠĄė×Ó¼ü B£®µ„ÖŹµÄ·Ö×ÓÖŠ¾ł²»“ęŌŚ»Æѧ¼ü
C£®ŗ¬ÓŠ¹²¼Ū¼üµÄ»ÆŗĻĪļŅ»¶ØŹĒ¹²¼Ū»ÆŗĻĪļ D£®ČĪŗĪĪļÖŹÄŚ¶¼ŗ¬ÓŠ»Æѧ¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ
£Ø1£©Ä³ĘųĢ¬Ńõ»ÆĪļ»ÆѧŹ½ĪŖRO2£¬ŌŚ±ź×¼×“æöĻĀ£¬1.28 gøĆŃõ»ÆĪļµÄĢå»żĪŖ448 mL£¬ŌņøĆŃõ»ÆĪļµÄĦ¶ūÖŹĮæĪŖ____________£¬RµÄĻą¶ŌŌ×ÓÖŹĮæĪŖ____________”£
£Ø2£©ŅŃÖŖCO”¢CO2µÄ»ģŗĻĘųĢåµÄÖŹĮæĪŖ15 g£¬ŌŚ±ź×¼×“æöĻĀĢå»żĪŖ8.8 L£¬ŌņæÉĶĘÖŖøĆ»ģŗĻĘųĢåÖŠŗ¬CO________ g£¬Ėłŗ¬CO2ŌŚ±ź×¼×“æöĻĀĢå»żĪŖ____________ L”£
£Ø3£©½«4 g NaOHČÜÓŚ____________gĖ®ÖŠ£¬²ÅÄÜŹ¹Ćæ100øöĖ®·Ö×ÓÖŠČÜÓŠ1øöNa£«”£
£Ø4£©Ķ¬ĪĀĶ¬Ń¹ĻĀSO2 Óė HeĆܶČÖ®±ČĪŖ £¬ČōÖŹĮæĻąµČ£¬Į½ÖÖĘųĢåµÄĢå»żÖ®±Č____________
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com