
| A、溶液中Cu2+向阳极移动,Cl-向阴极移动 |
| B、阳极上发生还原反应,阴极上发生氧化反应 |
| C、阴极反应:Cu2++2e-=Cu |
| D、可以用湿润的KI淀粉试纸检验阴极产生气体为Cl2 |


 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
| A、总反应为NO+NO2+O2+H2O═2HNO3 |
| B、总反应为4NO+8NO2+5O2+6H2O═12HNO3 |
| C、生成硝酸的物质的量浓度接近0.03 mol/L |
| D、生成硝酸的物质的量浓度约为0.45 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
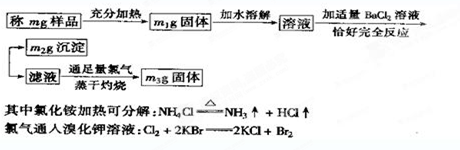
查看答案和解析>>
科目:高中化学 来源: 题型:

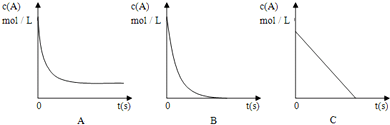
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25% | B、34% |
| C、75% | D、50% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,Na2CO3生成的CO2多 |
| B、两者的水溶液都是呈现碱性,可以使无色的酚酞变红色 |
| C、加热时,Na2CO3难分解,但NaHCO3容易分解 |
| D、同温度下,Na2CO3在水中的溶解度比NaHCO3大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.24L |
| B、4.48L |
| C、6.40L |
| D、12.8L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A、前5s的平均反应速率v(A)=0.03 mol?L-1?s-1 |
| B、前15s内体系的熵值逐渐增大 |
| C、保持温度不变,起始时向容器中充入2.0mol C,达平衡时,C的转化率大于80% |
| D、保持温度不变,起始时向容器中充入0.20mol A、0.20mol B和1.0mol C,反应达平衡前v(正)<v(逆) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com