
【题目】下列说法中正确的是 ![]()
![]()
A.主族元素的电负性越大,元素原子的第一电离能一定越大
B.在形成化合物时,电负性越小的元素越容易显负价
C.在元素周期表中,处于非金属三角区边缘的元素常被成称半金属
D.在元素周期表中,元素的原子半径从左到右逐渐增大
科目:高中化学 来源: 题型:
【题目】N2O5是一种新型硝化剂,一定温度下发生2N2O5(g)![]() 4NO2(g)+O2(g) ΔH>0,T1温度下的部分实验数据为
4NO2(g)+O2(g) ΔH>0,T1温度下的部分实验数据为
t/s | 0 | 500 | 1 000 | 1 500 |
c(N2O5)mol/L | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是( )
A. 500 s内N2O5分解速率为2.96×10-3 mol/(L·s)
B. T1温度下的平衡常数为K1=125,1 000 s时转化率为50%
C. 其他条件不变时,T2温度下反应到1 000 s时测得N2O5(g)浓度为2.98 mol/L,则T1<T2
D. T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1>K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S2O3是一种弱酸,实验室欲用0.01 mol·L-1的Na2S2O3溶液滴定I2溶液,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,下列说法合理的是

A. 该滴定可用甲基橙做指示剂
B. Na2S2O3是该反应的还原剂
C. 该滴定可选用右图所示装置
D. 该反应中每消耗2mol Na2S2O3,电子转移数为4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的分子式为![]() ,A属于第ⅥA族元素,B属于第ⅦA族元素,A和B在同一周期,它们的电负性分别为
,A属于第ⅥA族元素,B属于第ⅦA族元素,A和B在同一周期,它们的电负性分别为![]() 和
和![]() ,已知
,已知![]() 分子的键角为
分子的键角为![]() 。下列推断不正确的是
。下列推断不正确的是 ![]()
![]()
A.![]() 分子的空间构型为V形
分子的空间构型为V形
B.![]() 键为极性共价键,
键为极性共价键,![]() 分子为非极性分子
分子为非极性分子
C.![]() 分子中A原子采取
分子中A原子采取![]() 杂化
杂化
D.![]() 分子中无H原子,分子间不能形成氢键
分子中无H原子,分子间不能形成氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了某短周期元素R的各级电离能数据![]() 用
用![]() 、
、![]() 表示,单位为
表示,单位为![]() 。下列关于元素R的判断中一定正确的是
。下列关于元素R的判断中一定正确的是 ![]()
![]()
|
|
|
|
|
|
|
R | 740 | 1500 | 7700 | 10500 | 13600 |
|
a.![]() 的最高正价为
的最高正价为![]() 价
价
b.![]() 元素位于元素周期表中第ⅡA族
元素位于元素周期表中第ⅡA族
c.![]() 元素第一电离能大于同周期相邻元素
元素第一电离能大于同周期相邻元素
d.![]() 元素的原子最外层共有4个电子
元素的原子最外层共有4个电子
e.![]() 元素基态原子的电子排布式为
元素基态原子的电子排布式为![]()
A.acB.bcC.bcdD.bce
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用AG表示溶液的酸碱度,AG=![]() 。25℃,用0.100mol·L-1NaOH液滴定20.00 mL 0.100 mol·L-1 HNO2溶液, AG与所加NaOH溶液的体积(V)关系如图所示。下列说法不正确的是
。25℃,用0.100mol·L-1NaOH液滴定20.00 mL 0.100 mol·L-1 HNO2溶液, AG与所加NaOH溶液的体积(V)关系如图所示。下列说法不正确的是
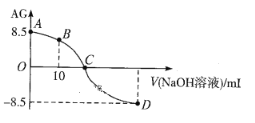
A. D点溶液中的pH=11.25
B. B点溶液中存在2c(H+)-2c(OH-)=c(NO2-)-c(HNO2)
C. C点时,加入NaOH溶液的体积小于20.00 mL
D. 25℃时,HNO2的电离平衡常数Ka=1.0×10-5.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2、NOx的含量是衡量大气污染的一个重要指标。工业上常采用催化还原法或吸收法处理SO2,催化还原SO2不仅可以消除SO2污染,而且可以得到有价值的中单质硫,采取氨水吸收NOx的方法去除NOx的污染,生成硝酸按。
(1)已知CH4和S的燃烧热分别为a kJ/mol和bkJ/mol。在复合组分催化剂作用下,甲烷可使SO2转化为S,同时生成CO2和液态水,该反应的热化方程式为___________。
(2)用H2还原SO2生成S的反应分两步完成,如图甲所示,该过程中相关物质的物质的量浓度随时间的变化关系如图乙所示:
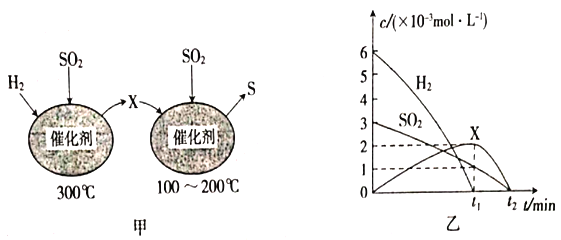
分析可知X为____________(写化学式);0-t1时间段的反应温度为____________,0-t1时间段用SO2表示的化学反应速率为______________________。
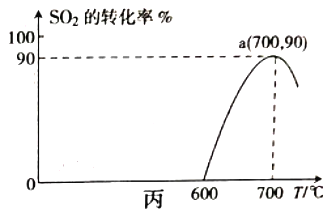
(3)焦炭催化还原SO2生成S2的化学方程式为 2C(s)+2SO2 (g)=S2(g)+2CO2(g)。在恒容容器中,浓度为1mol/L的SO2与足量焦炭反应,SO2的转化率随温度的变化如图丙所示。700℃时该反应的平衡常数为____________。
(4)25℃时,用1mol/L的Na2SO3溶液吸收SO2,当溶液的pH=7时,溶液中各离子浓度的大小关系为_____________。(已知:H2SO3的电离常数Ka1=1.3×10-2,Ka2=6.2×10-8)
(5)利用双离子交换膜电解法可以从含硝酸铵的工业废水里生产硝酸和氨。阳极室得到的物质是______,写出阳极反应方程式_______________________;阴极室得到的物质是_____________,写出阴极反应及获得相应物质的方程式______________、________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1.000 mol·L-1盐酸滴入20.00 mL 1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是
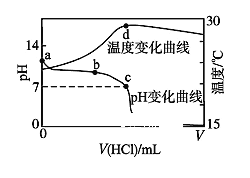
A. a点由水电离出的c(OH-)=1.0×10-14 mol·L-1
B. b点:c(NH4+)+c(NH3·H2O)=c(Cl-)
C. c点:c(Cl-)>c(NH4+)
D. d点:达到滴定终点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.2-甲基丁烷也称异丁烷B.烷烃 的正确命名是2-甲基-3-丙基戊烷
的正确命名是2-甲基-3-丙基戊烷
C.C4H9Cl有3种同分异构体D.三元轴烯(![]() )与苯互为同分异构体
)与苯互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com