
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| KSP | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
分析 I.(1)海水中的弱酸根离子水解显碱性;
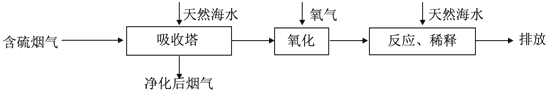
(2)H2SO3或HSO3-中的S显+4价,均可被O2氧化生成H+、SO42-,酸性会大大增强,氧化后的“海水”需要引入大量的显碱性的海水与之混合后才能排放,主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+);
II.(3)溶度积越小越易转化为沉淀,根据表格中的数据进行判断最近试剂;
(4)先计算出溶液中氢氧根离子的物质的量浓度,然后根据Pb(OH)2的溶度积及c(Pb2+)=$\frac{{K}_{sp}}{{C}^{2}(O{H}^{-})}$进行计算;
(5)根据氯化银的溶度积进行解答,并与排放标准对比来说明是否符合排放标准.
解答 解:I.(1)海水中主要含有Na+、K+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO-3等离子,在这些离子中能发生水解的是CO32-、HCO-3离子,CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-它们水解呈碱性,所以天然海水的pH≈8,呈弱碱性,
故答案为:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-;
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,氧气将H2SO3氧化为硫酸,该反应为2H2SO3+O2=2H2SO4,氧化后的“海水”需要用大量的天然海水与之混合后才能排放,是因中和稀释经氧气氧化后海水中生成的酸(H+),
故答案为:2H2SO3+O2=2H2SO4;中和、稀释经氧气氧化后海水中生成的酸;
II.(3)溶度积越小的越易转化为沉淀,由表格中的数据可知,硫化物的溶度积小,则应选择硫化钠,故答案为:B;
(4)由Pb(OH)2的溶度积为1.2×10-15,pH=8.0,c(OH-)=10-6mol•L-1,则c(Pb2+)=$\frac{{K}_{sp}}{{C}^{2}(O{H}^{-})}$=$\frac{1.2×1{0}^{-15}}{(1{0}^{-6})^{2}}$=1.2×10-3mol•L-1,
故答案为:1.2×10-3mol•L-1;
(5)废水中NaCl的质量分数为0.117%(ρ≈1g•mL-1),c(Cl-)=c(NaCl)=$\frac{1000×1g/mL×0.117%}{58.5g/mol}$=0.02mol/L,
Ksp(AgCl)=c(Ag+)•c(Cl-)=1.8×10-10mol2•L-2,则c(Ag+)=$\frac{1.8×1{0}^{-10}}{0.02}$=9×10-9mol•L-1,环境要求排放标准为c(Ag+)低于1.0×10-8mol•L-1,显然9×10-9mol•L-1<1.0×l0-8mol•L-1,则符合排放标准,
故答案为:9×10-9mol•L-1;是.
点评 本题考查了海水中资源的综合应用、含硫烟气的处理及难溶物的沉淀转化,侧重于考查学生对基础知识的综合应用能力,注意把握Ksp的有关计算的方法,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 氧化→加成→水解 | B. | 消去→加成→水解 | C. | 水解→消去→加成 | D. | 取代→水解→还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铜与盐酸、氢氧化钡与盐酸 | |
| B. | 石灰石和硝酸溶液、石灰石与盐酸溶液 | |
| C. | BaCO3与HCl溶液、Na2CO3溶液NaHSO4 | |
| D. | 石灰水中通CO2、石灰水中通SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 | |
| B. | 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 | |
| C. | 蒸馏时蒸馏烧瓶中液体的体积不能超过其容积的规格,液体也不能蒸干 | |
| D. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酱油中添加含铁的营养强化剂 | B. | 饮料中添加塑化剂 | ||
| C. | 用甲醛浸泡海鲜 | D. | 用工业盐腌制腊肉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 锂锰电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4.溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答:
锂锰电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4.溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 LCCl4含有的分子数为NA个 | |
| B. | 500mL 1moL/L的盐酸溶液中含有的HCl分子数为0.5 NA个 | |
| C. | 将1L 2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA个 | |
| D. | 23gNa与O2反应生成Na2O和Na2O2的混合物,转移的电子数为 NA个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com