
 ���ݻ���Ϊ500mL��I���������ܱ������зֱ����l molN2��2.5molH2�����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣬������������ͬ������·�����ӦN2��g��+3H2��g��?2NH3��g����H��O��ʵ���÷�Ӧ�����е�t minʱN2�����������ͼ��ʾ������˵����ȷ���ǣ�������
���ݻ���Ϊ500mL��I���������ܱ������зֱ����l molN2��2.5molH2�����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣬������������ͬ������·�����ӦN2��g��+3H2��g��?2NH3��g����H��O��ʵ���÷�Ӧ�����е�t minʱN2�����������ͼ��ʾ������˵����ȷ���ǣ�������| A����v��H2��=3v��N2��ʱ������˵�����������еķ�Ӧ��ƽ��״̬ |
| B����t minʱ��һ���ﻯѧƽ��״̬���Ǣ�͢� |
| C����t minʱ��һ��û�дﻯѧƽ��״̬����I |
| D�����������еķ�Ӧ���ﵽƽ�������I�л�������ƽ����Է���������С |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���ڢ� | C���ۢ� | D���٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
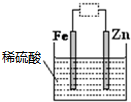
| A�����߿��н�ֱ����Դ�������ܻᱻ��ʴ |
| B�����߿��н����������ƻ��ֱ����Դ��п���Ǹ��� |
| C�����߿��н����������ƣ���װ�ÿɽ���ѧ��ת��Ϊ���� |
| D���������Һ�ij�����п��Һ������ֱ����Դ����װ�ÿ�������Ƥ�϶�п |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ֽ�ϲ���������ͼ���īˮ�ijɷ֣�Ϊ�˿���ɫ�ߣ�ֻ����ɫ���ӵļ���ſ�����ֽ������ |
| B������ƿ����Ͳ���ζ����϶��������ʹ���¶ȣ�����ƿ�б����ޡ�0���̶ȣ���Ͳ���ζ��ܶ��С�0���̶ȣ�ʹ��ʱ����ƿˮϴ������ϴ����Ͳ���ζ���ˮϴ������ϴ |
| C����ˮ�м��뱽����ˮ��ɫ������Ϊ���뱽������ȡ����Ӧ����ˮ��ͨ����ϩ����ˮ��ɫ������Ϊ������ϩ�����˼ӳɷ�Ӧ |
| D�����ʵķ����ᴿ����֮һΪ��ɸ�֡����罺��-�����������ᴿ����Һ-���˷��룬�����Ͼ����������������ӵ�ֱ����Сѡ����к��ʿ��ġ�ɸ�ӡ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ǹ��ۻ����� |
| B�������н�ǿ��ԭ�� |
| C����ͬλ��ԭ�ӹ��ɵ�ͬ���칹�� |
| D�����İ뾶H-С��Li+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������̿��SO2����ˮ��������������ԭ��Ӧ��ʹƷ����Һ��ɫ |
| B��Na2O2��H2O2������ѧ����ȫ��ͬ�������������� |
| C�������£�Ũ���ᡢŨ�����������ܷ����ۻ��������������� |
| D��ˮ�������ӷ��෨�ĽǶȣ��ɿ��������������ľ�ĵȵķ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 2 |
| 25 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
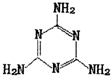 ��CN-����Ni2+�γ�[Ni��CN��4]2-������
��CN-����Ni2+�γ�[Ni��CN��4]2-�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ӧ��Ϊ������ԭ��Ӧ����Ӧ��Ϊ���ֽⷴӦ |
| B����Ӧ����Na2FeO4�ǻ�ԭ���� |
| C��Na2FeO4��FeΪ+6�ۣ�����ǿ�����ԣ���ɱ������ |
| D������2 mol FeCl3 ������Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ 6mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com