
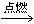 CO2£«2H2O£»C3H8£«5O2
CO2£«2H2O£»C3H8£«5O2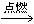 3CO2£«4H2O ĻÖÓŠŅ»Ģ×ŅŌŅŗ»ÆŹÆÓĶĘųĪŖŌĮĻµÄŌī¾ß£¬ÓūøÄĪŖÉÕĢģČ»Ęų£¬Ó¦²ÉČ”µÄ“ėŹ©ŹĒ£ŗ
3CO2£«4H2O ĻÖÓŠŅ»Ģ×ŅŌŅŗ»ÆŹÆÓĶĘųĪŖŌĮĻµÄŌī¾ß£¬ÓūøÄĪŖÉÕĢģČ»Ęų£¬Ó¦²ÉČ”µÄ“ėŹ©ŹĒ£ŗ[ ]

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013½ģø£½ØŹ”ČżĆ÷Ņ»ÖŠ”¢¶žÖŠøßČżÉĻѧʌʌĩĮŖæ¼»ÆѧŹŌ¾ķ£Ø“ų½āĪö£© ĢāŠĶ£ŗĢīæÕĢā
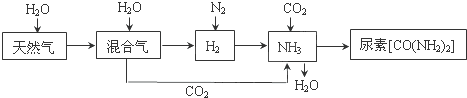
ŗĻ³É°±ÄņĖŲ¹¤ŅµÉś²ś¹ż³ĢÖŠÉę¼°µ½µÄĪļÖŹ×Ŗ»Æ¹ż³ĢČēĻĀĶ¼ĖłŹ¾”£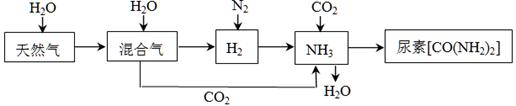
£Ø1£©ĢģČ»Ęų£ØÖ÷ŅŖ³É·ÖĪŖCH4£©ŌŚøßĪĀ”¢“߻ƼĮ×÷ÓĆĻĀÓėĖ®ÕōĘų·“Ӧɜ³ÉH2ŗĶCOµÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø2£©¼×ĶéŹĒŅ»ÖÖĒå½ąČ¼ĮĻ£¬µ«²»ĶźČ«Č¼ÉÕŹ±ČČŠ§ĀŹ½µµĶ£¬Ķ¬Ź±²śÉśÓŠ¶¾ĘųĢåŌģ³ÉĪŪČ¾”£
””ŅŃÖŖ£ŗCH4(g) + 2O2(g)£½CO2(g) + 2H2O(l)”” ””””¦¤H1£½ØD890.3 kJ/mol
2CO (g) + O2(g)£½2CO2(g)”””””””””””””” ¦¤H2£½ØD566.0 kJ/mol
Ōņ¼×Ķé²»ĶźČ«Č¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼ŗĶŅŗĢ¬Ė®Ź±µÄČČŠ§ĀŹŹĒĶźČ«Č¼ÉÕŹ±µÄ_____±¶£Ø¼ĘĖć½į¹ū±£Įō1Ī»Š”Źż£©”£
£Ø3£©¼×ĶéČ¼ĮĻµē³ŲæÉŅŌĢįÉżÄÜĮæĄūÓĆĀŹ”£ĻĀĶ¼ŹĒĄūÓĆ¼×ĶéČ¼ĮĻµē³Ųµē½ā50 mL 2 mol”¤L-1µÄĀČ»ÆĶČÜŅŗµÄ×°ÖĆŹ¾ŅāĶ¼£ŗ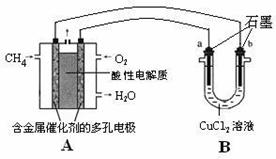 ””
””
Ēė»Ų“š£ŗ
¢Ł¼×ĶéČ¼ĮĻµē³ŲµÄÕż¼«·“Ó¦Ź½ŹĒ____ ____”£
¢Śµ±ĻßĀ·ÖŠÓŠ0.1 molµē×ÓĶعżŹ±£¬________£ØĢī”°a”±»ņ”°b”±£©¼«ŌöÖŲ________g”£
£Ø4£©ŌĖŹä°±Ź±£¬²»ÄÜŹ¹ÓĆĶ¼°ĘäŗĻ½šÖĘŌģµÄ¹ÜµĄ·§ĆÅ”£ŅņĪŖŌŚ³±ŹŖµÄ»·¾³ÖŠ£¬½šŹōĶŌŚÓŠNH3“ęŌŚŹ±Äܱ»æÕĘųÖŠµÄO2Ńõ»Æ£¬Éś³É[Cu(NH3)4]2+£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012-2013ѧğø£½ØŹ””¢¶žÖŠøßČżÉĻѧʌʌĩĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŗĻ³É°±ÄņĖŲ¹¤ŅµÉś²ś¹ż³ĢÖŠÉę¼°µ½µÄĪļÖŹ×Ŗ»Æ¹ż³ĢČēĻĀĶ¼ĖłŹ¾”£

£Ø1£©ĢģČ»Ęų£ØÖ÷ŅŖ³É·ÖĪŖCH4£©ŌŚøßĪĀ”¢“߻ƼĮ×÷ÓĆĻĀÓėĖ®ÕōĘų·“Ӧɜ³ÉH2ŗĶCOµÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø2£©¼×ĶéŹĒŅ»ÖÖĒå½ąČ¼ĮĻ£¬µ«²»ĶźČ«Č¼ÉÕŹ±ČČŠ§ĀŹ½µµĶ£¬Ķ¬Ź±²śÉśÓŠ¶¾ĘųĢåŌģ³ÉĪŪČ¾”£
””ŅŃÖŖ£ŗCH4(g) + 2O2(g)£½CO2(g) + 2H2O(l)”” ””””¦¤H1£½ØD890.3 kJ/mol
2CO (g) + O2(g)£½2CO2(g)”””””””””””””” ¦¤H2£½ØD566.0 kJ/mol
Ōņ¼×Ķé²»ĶźČ«Č¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼ŗĶŅŗĢ¬Ė®Ź±µÄČČŠ§ĀŹŹĒĶźČ«Č¼ÉÕŹ±µÄ_____±¶£Ø¼ĘĖć½į¹ū±£Įō1Ī»Š”Źż£©”£
£Ø3£©¼×ĶéČ¼ĮĻµē³ŲæÉŅŌĢįÉżÄÜĮæĄūÓĆĀŹ”£ĻĀĶ¼ŹĒĄūÓĆ¼×ĶéČ¼ĮĻµē³Ųµē½ā50 mL 2 mol”¤L-1µÄĀČ»ÆĶČÜŅŗµÄ×°ÖĆŹ¾ŅāĶ¼£ŗ
 ””
””
Ēė»Ų“š£ŗ
¢Ł¼×ĶéČ¼ĮĻµē³ŲµÄÕż¼«·“Ó¦Ź½ŹĒ____ ____”£
¢Śµ±ĻßĀ·ÖŠÓŠ0.1 molµē×ÓĶعżŹ±£¬________£ØĢī”°a”±»ņ”°b”±£©¼«ŌöÖŲ________g”£
£Ø4£©ŌĖŹä°±Ź±£¬²»ÄÜŹ¹ÓĆĶ¼°ĘäŗĻ½šÖĘŌģµÄ¹ÜµĄ·§ĆÅ”£ŅņĪŖŌŚ³±ŹŖµÄ»·¾³ÖŠ£¬½šŹōĶŌŚÓŠNH3“ęŌŚŹ±Äܱ»æÕĘųÖŠµÄO2Ńõ»Æ£¬Éś³É[Cu(NH3)4]2+£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗÄ£ÄāĢā ĢāŠĶ£ŗĢīæÕĢā


²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com