
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
分析 常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行共线、共面分析判断,注意单键可以旋转,以此解答该题.
解答 解:①丙烯CH2=CH-CH3中有一个甲基,甲基具有甲烷的结构特点,因此所有原子不可能处于同一平面上,故①错误;
②苯是平面结构,氟苯看作是一个氟原子取代苯中的一个氢原子,所有原子在同一个平面,故②正确;
③乙烯具有平面型结构,四氯乙烯看作是一个氯原子取代乙烯中的氢原子,所有原子在同一个平面,故③正确;
④甲苯中含有一个甲基,甲基具有甲烷的结构特点,因此所有原子不可能处于同一平面上,故④错误;
故选B.
点评 本题主要考查有机化合物的结构特点,为高频考点,侧重于学生的分析能力的考查,做题时注意从甲烷、乙烯、苯的结构特点判断有机分子的空间结构,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 30% | B. | 50% | C. | 70% | D. | 90% |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
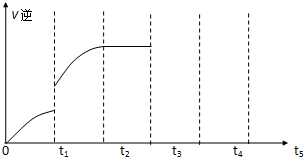
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
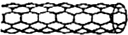
| A. | 纳米碳管是一种无机化合物 | |
| B. | 0.12g纳米碳管中含有6.02×l022个碳原子 | |
| C. | 纳米碳管与石墨互为同位素 | |
| D. | 纳米碳管中碳原子间以共价键结合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
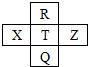 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )| A. | 非金属性:X<T<Z | B. | 第一电离能:Z<X<T | ||
| C. | 最高价氧化物的水化物酸性:Q<T<R | D. | 气态氢化物的还原性:R<T<X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li是最活泼金属,F是最活泼非金属 | |
| B. | Mg(OH)2碱性比Ca(OH)2强 | |
| C. | X2+的核外电子数目为18,则X在第三周期第ⅡA族 | |
| D. | 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{28}$<M<$\frac{1}{22.4}$ | B. | $\frac{1}{39.2}$<M<$\frac{1}{22.4}$ | C. | $\frac{1}{39.2}$<M<$\frac{1}{28}$ | D. | 0<M<$\frac{1}{22.4}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | I1 | I2 | I3 | I4 | I5 | I6 |
| 电力能 | 7.644 | 15.03 | 80.12 | 109.3 | 141.2 | 186.5 |
| 序号 | I7 | I8 | I9 | I10 | I11 | … |
| 电力能 | 224.9 | 266.0 | 327.9 | 367.4 | 1761 | … |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com