
773K时,将2.00 mol SO2和3.00 mol O2充入容积为10.00 dm3的密封容器中,平衡时有1.90 mol SO3生成。计算反应:2SO2(g) + O2(g) ![]() 2SO3(g) 的
2SO3(g) 的![]() 、
、![]() 以及SO2的转化率。
以及SO2的转化率。
分析:解此类题的关键是求出平衡时各物质的平衡浓度(或平衡分压)。反应时各物质的量变化之比,即为方程式中各物质的计量数之比。据此,根据起始浓度(或分压)即可求得各物质的平衡浓度(或平衡分压)。
解:根据题意,此反应是在等温等容条件下进行的。
2SO2 (g) + O2 (g) ![]() 2SO3 (g)
2SO3 (g)
起始浓度/ mol?dm3 2.00/10 3.00/10 0
变化浓度/ mol?dm3 1.90/10 ![]() ×1.90/10 +1.90/10
×1.90/10 +1.90/10
平衡浓度/ mol?dm3 ![]()

![]()
![]() =
=![]() = 1.8 × 103 dm3?mol
= 1.8 × 103 dm3?mol
![]() =
= ![]() (RT)
(RT)![]() = 1.8 × 103 dm3?mol1(8.31k Pa?dm3?mol1?K1×773K)23
= 1.8 × 103 dm3?mol1(8.31k Pa?dm3?mol1?K1×773K)23
SO2的转化率 = ![]() = 95.0 %
= 95.0 %


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源:0111 模拟题 题型:填空题
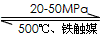 2NH3(g) △H=-192.0kJ·mol-1
2NH3(g) △H=-192.0kJ·mol-1 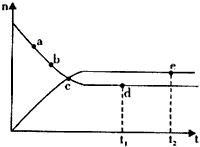
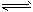 NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:_____________________。
NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:_____________________。 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com