
����Ŀ��R(OH)2��W(OH)2��������ˮ����R2+��W2+����ˮ��,������,R(OH)2��W(OH)2������Һ�������������ӵ�p(M2+)[p(M2+)=-lgc(M2+)]����ҺpH�ı仯��ϵ����ͼ��ʾ����֪��Ksp[R(OH)2]sp[W(OH)2]��������˵���д�������� ��
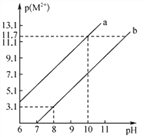
A. a�߱�ʾ������Һ��p(R2+ )����ҺpH�仯��ϵ
B. R(OH)2��W(OH)2�����������Һ�д���![]() =104.6
=104.6
C. ��������R(OH)2�ڱ���W(OH)2��Һ�е��ܽ�ȱ��ڴ�ˮ�е�С
D. ��RSO4��Һ�к�������W2+���ɼ�������RCO3��ȥW2+
���𰸡�D
�������������������Ksp[R(OH)2]<Ksp[W(OH)2]��֪����R2+��W2+�����ʵ���Ũ����ͬʱ��R2+�����ڽ�С��pH����������a�߱�ʾ������Һ��p(R2+)����ҺpH�仯��ϵ��pH=10ʱ��c(OH-)=![]() mol/L��c(R2+)=
mol/L��c(R2+)=![]() mol/L ������Ksp[R(OH)2]=
mol/L ������Ksp[R(OH)2]=![]() ��pH=8ʱ��c(OH-)=
��pH=8ʱ��c(OH-)=![]() mol/L��c(W2+)=
mol/L��c(W2+)=![]() mol/L ������Ksp[W(OH)2]=
mol/L ������Ksp[W(OH)2]=![]() ��A. ��Ksp[R(OH)2]<Ksp[W(OH)2]��֪����R2+��W2+�����ʵ���Ũ����ͬʱ��R2+�����ڽ�С��pH����������a�߱�ʾ������Һ��p(R2+)����ҺpH�仯��ϵ��A��ȷ��B. R(OH)2��W(OH)2�����������Һ�д����Ż�ѧƽ��R2+��W(OH)2
��A. ��Ksp[R(OH)2]<Ksp[W(OH)2]��֪����R2+��W2+�����ʵ���Ũ����ͬʱ��R2+�����ڽ�С��pH����������a�߱�ʾ������Һ��p(R2+)����ҺpH�仯��ϵ��A��ȷ��B. R(OH)2��W(OH)2�����������Һ�д����Ż�ѧƽ��R2+��W(OH)2![]() W2+�� R(OH)2����ƽ�ⳣ��K��
W2+�� R(OH)2����ƽ�ⳣ��K��![]() =104.6��B��ȷ��C. �����£�R(OH)2�ڱ���W(OH)2��Һ�е��ܽ�ȱ��ڴ�ˮ�е�С����ΪR(OH)2���ܽ���ܵ�W(OH)2��Һ�е�OH�������ƣ�C��ȷ��D. ��Ϊ��֪��RCO3��WCO3�ܽ�ȵ���Դ�С�����ԣ����жϼ�������RCO3�Ƿ���Գ�ȥRSO4��Һ�к��е�����W2+��D����ȷ�� ����ѡD��
=104.6��B��ȷ��C. �����£�R(OH)2�ڱ���W(OH)2��Һ�е��ܽ�ȱ��ڴ�ˮ�е�С����ΪR(OH)2���ܽ���ܵ�W(OH)2��Һ�е�OH�������ƣ�C��ȷ��D. ��Ϊ��֪��RCO3��WCO3�ܽ�ȵ���Դ�С�����ԣ����жϼ�������RCO3�Ƿ���Գ�ȥRSO4��Һ�к��е�����W2+��D����ȷ�� ����ѡD��


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǹ�ҵ��ˮ����IJ������̣������й�˵����ȷ����
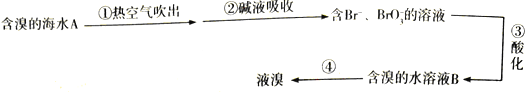
A. �������������ȿ��������dz��¿�����ԭ�����ȿ���������ǿ
B. ��Һ�����������Ļ�ѧ��Ӧ���������뻹ԭ��֮��Ϊ1 : 5
C. ���� �������ữ��Ҫ��ǿ�����Ե��ᣬ������
D. �����ˮ��ҺB�еĵ�����Ũ�ȱ�A�еĴ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£���a L HCl��ȫ����ˮ�õ�V mL���ᣬ��Һ���ܶ�Ϊ�� g��cm��3�����ʵ���������Ϊw�����ʵ����ʵ���Ũ��Ϊc mol��L��1��������������ȷ����
��c��![]() ��100%����c��
��100%����c��![]() ������������Һ���ټ���V mLˮ��������Һ��������������0.5w���ܽ�50 g������Һ����һ������ˮϡ�ͳ�0.5c mol��L��1�������ˮ�����Ӧ����50 mL
������������Һ���ټ���V mLˮ��������Һ��������������0.5w���ܽ�50 g������Һ����һ������ˮϡ�ͳ�0.5c mol��L��1�������ˮ�����Ӧ����50 mL
A. �٢� B. �ڢ�
C. �٢� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016��ȹ��ҿ�ѧ�����������ҹ�ŵ����������������ϣ��Ա������ڿ�ű�������ط�����о���
���������ϡ�������Ϊ��ɫ��״���壬�۵�156~157�棬�����ڱ�ͪ���ȷºͱ�����ˮ�������ܡ�
I.ʵ������������ȡ�����صĹ����������£�

��1���ڲ���IǰҪ��������з��飬��Ŀ����__________________��
��2������II��������_____________��
��3������III���е����ؽᾧ�����������Ϊ__________________________��
II����֪��������һ�����ĺ��������Ϊȷ���Ļ�ѧʽ���н���������ʵ�飺
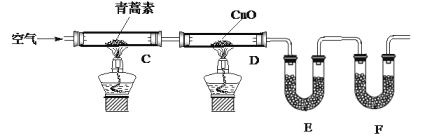
ʵ�鲽�裺
������װ�ã����װ�õ������ԡ�
�� ����E��F��������ҩƷ������
��ȡ14.10g�����ط���Ӳ���Թ�C�У���ȼC��D���ƾ��Ƽ��ȣ����ȼ��
��ʵ���������ȴ�����£�������Ӧ��E��F��������ҩƷ������
��4��װ��E��FӦ�ֱ�װ���ҩƷΪ_______________��___________________��
��5��ʵ���ã�
װ�� | ʵ��ǰ | ʵ��� |
E | 24.00g | 33.90g |
F | 100.00g | 133.00g |
ͨ��������������ص���Է�������Ϊ282������������ݣ��ó������صķ���ʽΪ______��
��6����ʹ����������������ϴ�ʵ������ĸĽ�������________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽ��������������Na2SO4��ˮ��ԭ����ͼ��ʾ�����ö��Ե缫��ab��cd��Ϊ���ӽ���Ĥ����ֱ���糡�������£���Ĥ�м��Na+��SO42-��ͨ�����ӽ���Ĥ�������˸��������ӱ��赲���ܽ����м���ҡ�����������ȷ����

A. ͨ����м���ҵ�SO42-����������Ǩ�ƣ���������ҺpH����
B. �÷��ڴ�����Na2SO4��ˮʱ���Եõ�NaOH��H2SO4��Ʒ
C. ������ӦΪ2H2O�C4e�C=O2+4H+����������ҺpH����
D. ����·��ͨ��1mol���ӵĵ���ʱ������0.5mol��O2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Fe��Cu�Ļ����Ͷ�뺬��Fe2+��Cu2+��Fe3+����Һ�У���Ӧ������ʣ�࣬�������ڻ�Ӧ���ڵ�����( )
A.Fe3+��Fe2+B.Fe2+��Cu2+C.Cu��Fe2+D.Cu��Cu2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���� �� ��
A. ���ۺ���ά�ض��Ǵ�����
B. ��֬������ʹ������Ȼ�̼��Һ��ɫ
C. ���Ǻ͵��۶�����ʹ����������ͭ�ڼ��������»�ԭ�ɺ�ɫ����
D. ��ë��������Ҫ�ɷֶ��ǵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ӣ�Ni-Cd���ɳ�������ִ��������й㷺Ӧ�á���֪ij���ӵ�صĵ������ҺΪKOH��Һ����䡢�ŵ簴��ʽ���У�Cd + 2NiOOH + 2H2O![]() Cd(OH)2 + 2Ni(OH)2���йظõ�ص�˵����ȷ����
Cd(OH)2 + 2Ni(OH)2���йظõ�ص�˵����ȷ����
A. ���ʱ������Ӧ��Ni(OH)2 ��e�� + OH- == NiOOH + H2O
B. �������ǻ�ѧ��ת��Ϊ���ܵĹ���
C. �ŵ�ʱ����������Һ�ļ��Բ���
D. �ŵ�ʱ�������Һ�е�OH-�������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��Һ����س��ʱ��̣���������ǿ������Ϊ��������ء�������ԭ����ͼ1��ʾ����Ӧ�����ӷ���ʽΪ:VO2++V3++H2O![]() VO2++V2++2H+���Դ˵�ص��Na2SO3��Һ(�缫����Ϊʯī),������NaOH��ͬʱ�õ�H2SO4����ԭ����ͼ2��ʾ������˵���������
VO2++V2++2H+���Դ˵�ص��Na2SO3��Һ(�缫����Ϊʯī),������NaOH��ͬʱ�õ�H2SO4����ԭ����ͼ2��ʾ������˵���������
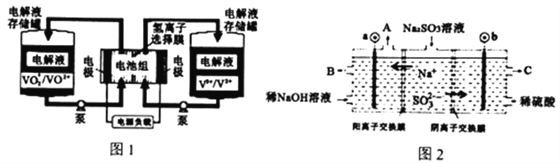
A. ���Na2SO3��Һʱ,a�����ظ�������,ͼ1��H+�ӵ���ұ��������
B. ��س��ʱ,�����缫��ӦΪVO2++e-+2H+=VO2++H2O
C. ���ʱb�ĵ缫��ӦʽΪSO32-+H2O-2e-=SO42-+2H+
D. ����������ͼ2����Һ��������ܱգ�������12.6gNa2SO3,�������仯������Ϊ4.4g
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com