
【题目】现有A、B、C、D、E、F六种短周期主族元素,原子序数依次增大.已知A的气态氢化物能与其最高价氧化物的水化物反应,B原子最外层电子数是电子层数的3倍,C+和D3+离子的电子层结构相同,B与E属于同一主族.请回答下列问题:

(1)E在元素周期表中的位置是________
(2)上述元素形成的简单离子中,半径最小的是________(填离子符号).
(3)由上述元素中的一种或几种组成的物质甲可以发生如图1反应:
①若乙具有漂白性,则乙的电子式为________.
②若丙的水溶液是强碱性溶液,则甲为______________(填化学式).
③若乙为二元弱酸,丙既能溶于强酸、又能溶于强碱,则乙的名称为________;用电离方程式表示丙既能溶于强酸、又能溶于强碱的原因________.
④乙遇空气变为红棕色,有同学认为“浓硫酸可以干燥气体甲”,为验证其观点是否正确.用如图2装置进行实验时,分液漏斗中应加入________(填试剂名称).实验过程中,浓硫酸中未发现有气体逸出,且溶液变为红棕色,由此得出的结论是________.
【答案】 第三周期第VIA族 Al3+ ![]() Na或Na2O2 硫化氢或氢硫酸 AlO2﹣+H2O+H+Al(OH)3Al3++3OH﹣ 浓硝酸 ;浓硫酸不能干燥二氧化氮或二氧化氮能溶于浓硫酸
Na或Na2O2 硫化氢或氢硫酸 AlO2﹣+H2O+H+Al(OH)3Al3++3OH﹣ 浓硝酸 ;浓硫酸不能干燥二氧化氮或二氧化氮能溶于浓硫酸
【解析】A、B、C、D、E、F六种短周期主族元素,原子序数依次增大,A的气态氢化物能与其最高价氧化物的水化物反应,则A是N元素;B原子最外层电子数是电子层数的3倍,B为O元素;B与E属于同一主族,则E是S元素;F为短周期主族元素且原子序数大于E,则F为Cl元素;![]() 和
和![]() 离子的电子层结构相同,为第三周期元素,C、D分别为Na、Al元素。
离子的电子层结构相同,为第三周期元素,C、D分别为Na、Al元素。
(1)E是S元素,S原子核外电子层数等于其周期数、最外层电子数等于其族序数,S原子核外有3个电子层、最外层电子数是6,所以S位于第三周期第VIA族;正确答案:第三周期第VIA族。
(2)上述元素形成的简单离子中,电子层数越少的原子半径越小,电子层结构相同的离子,离子半径随着原子序数增大而减小,这几种元素形成的离子半径大小顺序是![]() P,所以离子半径最小的是
P,所以离子半径最小的是![]() ,正确答案:
,正确答案:![]() 。
。
(3)①若乙具有漂白性,为HClO,则甲是氯气、丙是HCl,HClO分子中O原子和H、Cl原子之间分别共用一对电子,电子式为:![]() ;正确答案:
;正确答案:![]() 。
。
②若丙的水溶液是强碱性溶液,则甲为Na或![]() ,丙为NaOH,乙为氢气或氧气,正确答案:Na或
,丙为NaOH,乙为氢气或氧气,正确答案:Na或![]() 。
。
③若乙为二元弱酸,丙既能溶于强酸、又能溶于强碱,丙为氢氧化铝;乙为硫化氢,则甲是硫化铝,乙名称为硫化氢或氢硫酸,氢氧化铝能发生酸式电离也能发生碱式电离,电离方程式为AlO2﹣+H2O+H+Al(OH)3Al3++3OH﹣,所以氢氧化铝能溶于强碱和强酸溶液;正确答案:硫化氢或氢硫酸; AlO2﹣+H2O+H+Al(OH)3Al3++3OH﹣。
④用如图2装置进行实验时,浓硝酸和Cu反应生成二氧化氮,所以分液漏斗中液体是浓硝酸;实验过程中,浓硫酸中未发现有气体逸出,且溶液变为红棕色,则二氧化氮溶于浓硫酸,说明二氧化氮能溶于浓硫酸或浓硫酸不能干燥二氧化氮;正确答案:浓硝酸;浓硫酸不能干燥二氧化氮或二氧化氮能溶于浓硫酸。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】2016年诺贝尔化学奖由法国、美国、荷兰的三位科学家获得,表彰他们在“分子机器的设计与合成”做出的贡献。下列物质由分子构成且属于电解质的是
A.H2SO4 B.NaCl C.NH3 D.Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiPF6是锂离子电池中广泛应用的电解质。某工厂用LiF、PCl5为原料,低温反应制备LiPF6。其流程如下:
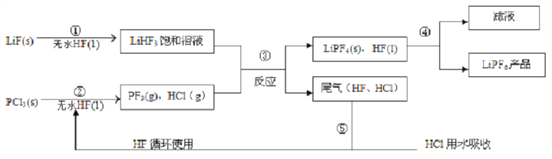
已知:HCl的沸点是-85.0℃,HF的沸点是19.5℃。
(1)第①步反应中无水HF的作用是________、__________。反应设备不能用玻璃材质的原因是______________(用化学方程式表示)。无水HF有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的____________溶液冲洗。
(2)该流程需在无水条件下进行,第③步反应中PF5极易水解,其产物为两种酸,写出PF5水解的化学方程式:________________。
(3)第④步分离采用的方法是_____________;第⑤步分离尾气中HF、HC1采用的方法是____________。
(4)LiPF6产品中通常混有少量LiF。取样品wg。测得Li的物质的量为nmol,则该样品中LiPF6的物质的量为__________mol(用含有w、n的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】家用天然气的主要成分是烷烃,其中甲烷(CH4)占绝大多数,已知氧气约占空气体积的20%,出现燃气泄漏时如果遇到火花会引起爆炸,当泄漏的甲烷与空气体积比为1:10时,爆炸最剧烈,此时甲烷与氧气的质量比约为
A.1:2B.2:1C.1:4D.4:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用A+、B﹣、C2﹣、D、E、F分别表示含有18个电子的几种微粒(离子或分子),请回答下列问题:
(1)A元素是________、B元素是________、C元素是________(用元素符号表示).
(2)D是由两种元素组成的双原子分子,用电子式表示其形成过程________.
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是________,其与水反应的化学方程式为________.
(4)F分子中含有6个原子,其化学式是________或________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸镧[La2(CO3)3]可用于治疗终末期肾病患者的高磷酸盐血症。制备反应原理为:LaCl3+6NH4HCO3= La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O;某化学兴趣小组利用下列装置实验室中模拟制备碳酸镧。
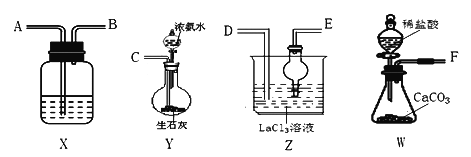
(1)盛放稀盐酸的仪器为__________________。
(2)制备碳酸镧实验流程中导管从左向右的连接顺序为:F→ → → → → 。_____________
(3)Y中发生反应的化学反应式为____________________________________。
(4)X中盛放的试剂是____________,其作用为___________________________。
(5)Z中应先通入NH3,后通入过量的CO2,原因为_________________________。
(6)La2(CO3)3质量分数的测定:准确称取10.0g产品试样,溶于10.0mL稀盐酸中,加入10 mL NH3-NH4Cl缓冲溶液,加入0.2 g紫脲酸铵混合指示剂,用0.5 mol·L-1 EDTA(Na2H2Y)标准溶液滴定至呈蓝紫色(La 3++H2Y2-= LaY-+2H+),消耗EDTA溶液44.0 mL。则产品中La2(CO3)3的质量分数w[La2(CO3)3]=________________。
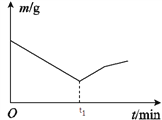
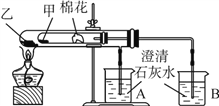
(7)该化学兴趣小组为探究La2(CO3)3和La(HCO3)3的稳定性强弱,设计了如下的实验装置,则甲试管中盛放的物质为__________;实验过程中,发现乙试管中固体质量与灼烧时间的关系曲线如图所示。在t1 min之后固体质量增加的原因可能是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废水中含有CN-和Cr2O72-等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
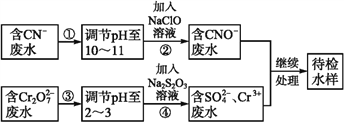
回答下列问题:
(1)步骤②中,CN-被ClO-氧化为CNO-的离子方程式为_______________。
(2)步骤④的反应为S2+Cr2O72-+H+![]() SO42-+Cr3++H2O(未配平), 则每消耗0.4 molCr2O72-转移转移____mol e-。
SO42-+Cr3++H2O(未配平), 则每消耗0.4 molCr2O72-转移转移____mol e-。
(3)含Cr3+废水可以加入熟石灰进一步处理,目的是_________________。
(4)在25 ℃下,将a mol·L-1的NaCN溶液与0.01 mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,用含a的代数式表示HCN的电离常数Ka=____。若25 ℃时将浓度均为0.1 mol·L-1的NaCN、HCN溶液等体积混合后,溶液呈碱性,则关于该溶液的说法不正确的是____(填字母)。
a.此溶液一定有c(Na+)+c(H+)=c(OH-)+c(CN-)
b.此溶液一定有c(Na+)=c(HCN)+c(CN-)
c.混合溶液中水的电离程度一定大于该温度下纯水的电离程度
d.此溶液加入少量氢氧化钠或盐酸,溶液的pH变化不大
(5)除去废水中的阳离子:取水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入一定量的Na2S溶液,蓝色沉淀转化成黑色沉淀。该过程中反应的离子方程式为_______、___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T K时,向2.0L恒容密闭容器中充入0.10molCOCl2,发生反应![]() ,经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是
,经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是

A. T K时该反应的化学平衡常数为![]()
B. 反应在前2s的平均速率![]() mol·L-1·s-1
mol·L-1·s-1
C. 保持其他条件不变,升高温度,若新平衡时c(C12)=0.038mol·L-1,则反应的△H<0
D. 平衡后向上述容器中再充入0.10molCOCl2,平衡正向移动,COCl2的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定质量的镁、铝混合物投到2molL﹣1的盐酸中,待金属完全溶解后,向溶液中加入2molL﹣1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示.则: 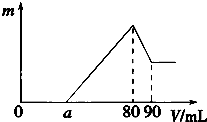
(1))80~90mL对应反应的离子方程式 .
(2)金属铝的质量为
(3)盐酸的体积是mL.
(4)a的取值范围是 .
(5)n(Mg)/n(Al)的最大值是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com