



 ȫ��������ϵ�д�
ȫ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
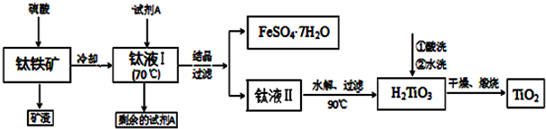
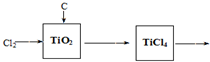
 ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ��A����һ��ֲ���������ڼ���A�ɷ�����ͼ��ʾ��һϵ�л�ѧ��Ӧ����ͼ�ش��������⣺
ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ��A����һ��ֲ���������ڼ���A�ɷ�����ͼ��ʾ��һϵ�л�ѧ��Ӧ����ͼ�ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ��ʾ������·��ͨʱ������M������ɫʯ����Һ��������ֽ��a������ɫ��b���Ժ�ɫ����֪���е缫������п-�������е缫�����Dz�-ͭ �����������������仯���ش�
��ͼ��ʾ������·��ͨʱ������M������ɫʯ����Һ��������ֽ��a������ɫ��b���Ժ�ɫ����֪���е缫������п-�������е缫�����Dz�-ͭ �����������������仯���ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | ʵ�� | ���� |
| A | ����ˮ��Ӧ | �����Ӵ�ú����ȡ�������ƣ����������̶���С���ƣ�����װ��ˮ���ձ��� |
| B | ������ˮ��ȡ����ˮ | ��������ƿ�м�����������ˮ�ͼ�����ʯ�����Ӻ�װ�ã�����������ƿ������ƿ�ռ�������Һ�� |
| C | ��ȥ�Ȼ�þ��Һ�л��е������Ȼ��� | �������������������Һ����ȫ��Ӧ����ˣ�������ϴ�Ӻ��������ǡ���ܽ� |
| D | ����һ��Ũ�ȵ��Ȼ�����Һ1000mL | ȷ��ȡ�Ȼ��ع��壬���뵽1000ml������ƿ�У���ˮ�ܽ⣬��ҡ�ȣ����� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��S��s��+O2��g��=SO2��g������H=-297.23kJ?mol-1 |
| B��2H2��g��+O2��g��=2H2O��1������H=-571.6 kJ |
| C��CaCO3��s��=CaO��s��+CO2��g������H=178.5 kJ?mol |
| D��Zn+CuSO4��aq��=ZnSO4��aq��+Cu����H=-216kJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������ὦ�����У�Ӧ������ˮ��ϴ����ϴ��գ�۾� |
| B��������Ũ����Һմ��Ƥ���ϣ�Ҫ�����ô���ˮ��ϴ��Ȼ��Ϳ��������Һ |
| C����ú����ȡ�ý����Ʊ��������ӣ��������ִ��� |
| D������������Һʱ����������Ͳ�м���һ�������ˮ�����ڽ�������������Ũ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����FeBr2��Һ��ͨ��������Cl2��2Fe2++Cl2�T2Fe3++2Cl- |
| B����NH4Al��SO4��2��Һ�е���Ba��OH��2ǡ��ʹSO42-��Ӧ��ȫ2Ba2++4OH-+Al3++2SO42-+NH4+�T2BaSO4��+Al��OH��3��+NH3��H2O |
| C����Mg��HCO3��2��Һ�м�������� NaOH��ҺMg2++2HCO3-+2OH-�TMgCO3��+CO32-+2H2O |
| D����Fe��NO3��2��Һ�м���ϡ���3Fe2++4H++NO3-�T3Fe3++NO��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 25��ʱ����20ml 0.1mol?L-1NaOH��Һ����μ���0.2mol?L-1������Һ��������ͼ��ʾ���й�����Ũ�ȹ�ϵ�ıȽ��У�����ȷ���ǣ�������
25��ʱ����20ml 0.1mol?L-1NaOH��Һ����μ���0.2mol?L-1������Һ��������ͼ��ʾ���й�����Ũ�ȹ�ϵ�ıȽ��У�����ȷ���ǣ�������| A����A�㣺c��Na+����c��CH3COO-����c��OH-����c��H+�� |
| B����B�㣺c��Na+��=c��CH3COO-����c��OH-��=c��H+�� |
| C����C�㣺c��Na+��+c��H+��=c��CH3COO-��+c��OH-�� |
| D����C�㣺c��Na+��=c��CH3COO-��+c��CH3COOH�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com